

���� ��1���ٸ���ʵ��Ŀ��֪��ʵ��װ������˳��Ϊ��������ȡװ�á�����װ�á�����װ�á�ˮ����װ�á���������װ�ã�
�ڳ�ȥ���������Ҳ��������µ����ʣ�������������ܺͽϻ��ý��������������ﷴӦ�����Σ�
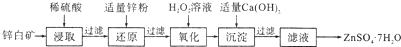
��2��п���м���ϡ�����ȡ��ZnO��Fe2O3��CuO�ֱ��ϡ���ᷴӦ����ZnSO4��Fe2��SO4��3��CuSO4��SiO2��ϡ�����Ӧ��Ȼ����ˣ��õ�����Һ�к���ZnSO4��Fe2��SO4��3��CuSO4��H2SO4������Һ�л���Zn����Fe3+��ԭΪFe2+���õ�Cu������Ȼ����ˣ��õ�����Һ�к���ZnSO4��FeSO4������Һ�м���˫��ˮ��˫��ˮ��Fe2+����ΪFe3+������Һ�м��������������ƣ���ҺpH���ߣ�������ת��Ϊ��������������������ˣ��õ�����Һ�к���ZnSO4������Һ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����õ�ZnS04•7H2O��
�������¶ȡ�����Ӧ��Ӵ��������������Ũ�ȶ�������Ӧ���ʣ�
�������Ӻ�Zn��Ӧ�����������Ӻ�п���ӣ�ͭ���Ӻ�п�����û���Ӧ��
��˫��ˮ����ǿ�����ԣ��ܽ�������������Ϊ�����ӣ�
�ܴ���Һ�л�ȡ�����������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����Ȳ�����
��� �⣺��1���ٸ���ʵ��Ŀ��֪��ʵ��װ������˳��Ϊ��������ȡװ�á�����װ�á�����װ�á�ˮ����װ�á���������װ�ã�A����ȡ������D�Ǹ���������B�Ǽ���������ԭ�ԡ�E�Ǽ�����������ˮ��C�Ǹ����������������˳����ADBEC��װ��E��ʢ�ŵ��Լ�Ϊ��ˮ����ͭ����Ŀ���Ǽ��������������Cװ�õ������Ƿ�ֹ������ˮ��������װ�ã�����������������ļ��飬
�ʴ�Ϊ��ADBEC����ˮ����ͭ����ֹ������ˮ��������װ�ã�����������������ļ��飻
�ڳ�ȥ���������Ҳ��������µ����ʣ�������������ܺͽϻ��ý��������������ﷴӦ�����Σ��Ȼ������������ƶ��������ʣ�ֻ��п�ܺ�ϡ���ᷴӦ�Ҳ��ܲ������ʣ��ʴ�Ϊ��������п�ۣ�
��2��п���м���ϡ�����ȡ��ZnO��Fe2O3��CuO�ֱ��ϡ���ᷴӦ����ZnSO4��Fe2��SO4��3��CuSO4��SiO2��ϡ�����Ӧ��Ȼ����ˣ��õ�����Һ�к���ZnSO4��Fe2��SO4��3��CuSO4��H2SO4������Һ�л���Zn����Fe3+��ԭΪFe2+���õ�Cu������Ȼ����ˣ��õ�����Һ�к���ZnSO4��FeSO4������Һ�м���˫��ˮ��˫��ˮ��Fe2+����ΪFe3+������Һ�м��������������ƣ���ҺpH���ߣ�������ת��Ϊ��������������������ˣ��õ�����Һ�к���ZnSO4������Һ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����õ�ZnS04•7H2O��
�������¶ȡ�����Ӧ��Ӵ��������������Ũ�ȶ�������Ӧ���ʣ�Ϊ��������Ч�ʣ����Բ�ȡ�Ĵ�ʩ�н���۷��顢����¶Ȼ��ʵ��������Ũ�ȵȣ��ʴ�Ϊ������۷��顢����¶Ȼ��ʵ��������Ũ�ȵȣ�
�������Ӻ�Zn��Ӧ�����������Ӻ�п���ӣ�ͭ���Ӻ�п�����û���Ӧ�����Լ���п�۵�Ŀ���dz�ȥͭ����ͬʱ��������ת��Ϊ�������ӣ��ʴ�Ϊ����ȥͭ����ͬʱ��������ת��Ϊ�������ӣ�
��˫��ˮ����ǿ�����ԣ��ܽ�������������Ϊ�����ӣ����ӷ���ʽΪH2O2+2Fe2++2H+=2Fe3++2H2O���ʴ�Ϊ��H2O2+2Fe2++2H+=2Fe3++2H2O��
�ܴ���Һ�л�ȡ�����������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����Ȳ������ʴ�Ϊ������Ũ������ȴ�ᾧ��
���� ���⿼�����ʷ�����ᴿ��ʵ��װ���ۺϵ�֪ʶ�㣬Ϊ��Ƶ���㣬��ȷ���ʵ����ʼ�ʵ�鲽���ǽⱾ��ؼ���֪������ͼ�з����ķ�Ӧ����������������ʵ���Ⱥ�˳��ȣ��ѵ��ǣ�1����װ��˳�����У���Ŀ�Ѷ��еȣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ | B�� | ���� | C�� | ���� | D�� | ø |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | һ�����������ӡ����ӡ�������ɵ� | |
| B�� | ��ѧ���ʼ�����ȫ��ͬ | |
| C�� | �˵�����ͺ��������һ����� | |
| D�� | ������һ����ͬ����������������һ������ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ������ˮ���ֻ������ͻ������ | |
| B�� | �������������ԭ�ӿ�����ͬһƽ�� | |
| C�� | ������������NaHCO3��Һ������Ӧ | |
| D�� | 1 mol��������������3 mol H2�����ӳɷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| n��SO32-����n��HSO3-�� | 91��9 | 1��1 | 1��91 |
| pH | 8.2 | 7.2 | 6.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
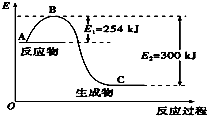 ���ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���ã�
���ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���ã�| ��ѧ�� | H-H | N��N |
| ����/kJ•mol-1 | 435 | 943 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ͬ����Ԫ�صĵ�һ�����ܱ仯���ƣ��Ƴ�Al�ĵ�һ�����ܱ�Mg�� | |
| B�� | ��������Ԫ����������ϼ����������Ĺ�ϵ���Ƴ�±��Ԫ��������۶���+7 | |
| C�� | ����ͬ����Ԫ�صĵ縺�Ա仯���ƣ��Ƴ�Ar�ĵ縺�Ա�Cl�� | |
| D�� | ���ݽ�ǿ�������ȡ������Ĺ��ɣ��Ƴ�CO2ͨ��NaClO��Һ��������HClO |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com