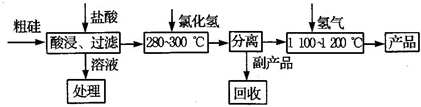
我国目前制备多晶硅主要采用三氯氢硅氢还原法、硅烷热解法和四氯化硅氢还原法.由于三氯氢硅还原法具有一定优点,被广泛应用.其简化的工艺流程如图所示:
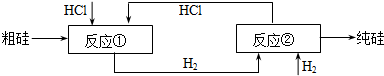
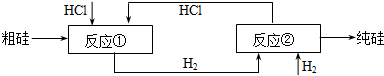
反应①:Si(粗)+3HCl(g)
SiHCl
3(l)+H
2(g)
反应②:SiHCl
3+H
2 Si(纯)+3HCl
(1)制备三氯氢硅的反应为:Si(s)+3HCl(g)═SiHCl
3(g)+H
2(g);△H=-210kJ?mol
-1.伴随的副反应有:Si(s)+4HCl(g)═SiCl
4(g)+2H
2(g);△H=-241kJ?mol
-1.SiCl
4在一定条件下与H
2反应可转化为SiHCl
3,反应的热化学方程式为:SiCl
4(g)+H
2(g)═SiHCl
3(g)+HCl(g);△H=
+31kJ?mol-1
+31kJ?mol-1
.
(2)假设在每一轮次的投料生产中,硅元素没有损失,反应①HCl中的利用率为75%,反应②中和H
2的利用率为80%.则在下一轮次的生产中,需补充投入HCl和H
2的体积比是
4:1
4:1
.
(3)由于SiH
4具有易提纯的特点,因此硅烷热分解法是制备高纯硅很有发展潜力的方法.工业上广泛采用的合成硅烷方法是让硅化镁和固体氯化铵在液氨介质中反应得到硅烷,化学方程式是
Mg2Si+4NH4Cl═SiH4↑+2MgCl2+4NH3↑
Mg2Si+4NH4Cl═SiH4↑+2MgCl2+4NH3↑
;
整个制备过程必须严格控制无水,否则反应将不能生成硅烷,而是生成硅酸和氢气等,其化学方程式为
Mg2Si+4NH4Cl+3H2O═2MgCl2+H2SiO3+4NH3↑+4H2↑
Mg2Si+4NH4Cl+3H2O═2MgCl2+H2SiO3+4NH3↑+4H2↑
;
整个系统还必须与氧隔绝,其原因是
由于硅烷在空气中易燃,浓度高时容易发生爆炸
由于硅烷在空气中易燃,浓度高时容易发生爆炸
.
(4)若将硅棒与铁棒用导线相连浸在氢氧化钠溶液中构成原电池,则负极的电极反应式为:
Si+6OH--4e-=SiO32-+3H2O
Si+6OH--4e-=SiO32-+3H2O
(5)硅能用于合成硅橡胶,右图是硅橡胶中的一种,其主要优点是玻璃化温度低,耐辐射性能好,则该硅橡胶的化学式为
(C24H18SiO2)n
(C24H18SiO2)n
.




 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案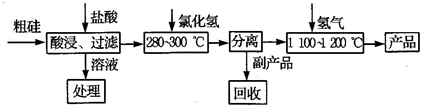


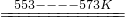 SiHCl3(l)+H2(g)
SiHCl3(l)+H2(g)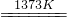 Si(纯)+3HCl
Si(纯)+3HCl