
| A、同时用食醋和酒烧菜,菜味更香 |
| B、蔗糖溶液中加入银氨溶液水浴加热,有银镜生成 |
| C、苯中碳碳键是介于C-C和C=C之间的一种特殊共价键 |
| D、反应2CrO3+3CH3CH2OH+3H2SO4═Cr2(SO4)3+3CH3CHO+6H2O可用于检验是否酒后驾驶,该反应中CrO3作氧化剂 |


科目:高中化学 来源: 题型:
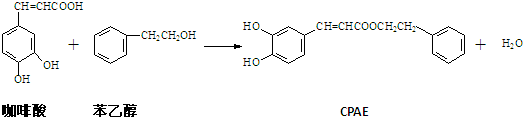
| A、1mol CPAE与足量的NaOH溶液反应,最多消耗3mol NaOH |
| B、可用金属Na检测上述反应是否残留苯乙醇 |
| C、与苯乙醇互为同分异构体的酚类物质共有9种 |
| D、咖啡酸可发生聚合反应,而且其分子中含有3种官能团 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子序数:X<Y |
| B、原子半径:X<Y |
| C、原子半径:X>Y |
| D、原子最外层电子数:X<Y |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、V(NaOH)=0时,c(H+)=1×10-2mol?L-1 |
| B、V(NaOH)<10mL时,可能存在c(Na+)=2c(C2O42-)+c(HC2O4-) |
| C、V(NaOH)=10mL时,c(H+)=1×10-7mol/L |
| D、V(NaOH)>10mL时,一定有c(Na+)>c(C2O42-)>c(OH-)>c(HC2O4-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Z、W、M形成的简单离子,其半径大小关系为Z>W>M |
| B、M的最高价氧化物对应的水化物与Y、W两元素最高价氧化物对应的水化物均能反应 |
| C、工业上可用电解熔融的W的氯化物的方法制取W单质 |
| D、Y、Z元素形成的简单氢化物的稳定性:Z>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙醇汽油是一种化合物 |
| B、汽车使用乙醇汽油可以减少有害气体的排放 |
| C、乙醇充分燃烧生成CO2和H2O |
| D、用粮食发酵可制得乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:
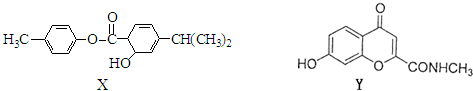
| A、1mol X与NaOH溶液反应,最多消耗2 mol NaOH |
| B、X、Y都有较强的水溶性 |
| C、X、Y都能使KMnO4溶液褪色 |
| D、X、Y的水解产物有可能发生聚合反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 加入NaOH溶液的体积 | pH | |
| ① | 0L | 2 |
| ② | 1L | 4 |
| ③ | 2L | 10 |
| ④ | 3L | 12 |
| c(Na+) | ||
c(P
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com