
【题目】某化学兴趣小组的同学为制取少量溴乙烷,查阅资料得知:
NaBr+H2SO4→HBr+NaHSO4
CH3CH2OH+HBr ![]() CH3CH2Br+H2O
CH3CH2Br+H2O
化学兴趣小组根据实验原理设计如图的装置.
根据题意完成下列填空:有关数据列表如下:
乙醇 | 溴乙烷 | |
状态 | 无色液体 | 无色液体 |
密度/gcm﹣3 | 0.8 | 1.4 |
沸点/℃ | 78.5 | 119.0 |
熔点/℃ | ﹣l30 | 38.4 |
(1)圆底烧瓶中加入的反应物是溴化钠、和2:1的硫酸.配制体积比2:1的硫酸所用的仪器为选填编号)
a.烧杯 b.玻璃棒 c.量筒 d.容量瓶 e.滴定管
(2)将生成物导入盛有冰水混合物的试管A中,试管A中的物质分为三层(如图所示),产物在第层;
(3)用浓的硫酸进行实验,若试管A中获得的有机物呈棕黄色,除去其中杂质应加入选填编号)然后再进行一步操作即可;
a.无水氯化钙 b.硝酸银溶液 c.四氯化碳 d.亚硫酸钠溶液
(4)实验过程中,同学发现仪器连接部分有漏气现象,老师建议把上述装置中的仪器连接部分都改成标准玻璃接口,其原因是:;
(5)假设最初取用的无水乙醇是57.5mL,最后得到的纯净的溴乙烷是52.0mL,则溴乙烷的产率为 .
【答案】
(1)乙醇;abc
(2)3
(3)d;分液
(4)反应会产生Br2 , 腐蚀橡胶
(5)66.8%
【解析】解:(1.)实验室制取少量溴乙烷所用试剂是乙醇和溴化氢反应,二者在加热下发生取代反应生成溴乙烷;配制体积比2:1的硫酸所用的仪器有烧杯、玻璃棒和量筒所以答案是:乙醇; abc;
(2.)生成的溴乙烷和水互不相溶,并且溴乙烷的密度比水大,在冰水混合物的下层,所以答案是:3;
(3.)试管A中获得的有机物呈棕黄色,是由于浓硫酸具有强氧化性,将HBr氧化物Br2 , 产物为溴乙烷,混有单质溴,蒸馏不能完全除去杂质,并且操作麻烦,氢氧化钠溶液易使溴乙烷水解,四氯化碳会引入新的杂质,而亚硫酸钠和溴发生氧化还原反应生成HBr和硫酸钠,易与溴乙烷分离,两者分层,用分液的方法分离,
所以答案是:d; 分液;
(4.)浓硫酸具有强氧化性,将HBr氧化物Br2 , 生成的Br2具有强氧化性,会腐蚀橡胶,应用玻璃导管,所以答案是:反应会产生Br2 , 腐蚀橡胶;
(5.)n(乙醇)= ![]() =1mol,n(溴乙烷)=
=1mol,n(溴乙烷)= ![]() =0.668mol,该反应的产率为:
=0.668mol,该反应的产率为: ![]() ×100%=66.8%,所以答案是:66.8%.
×100%=66.8%,所以答案是:66.8%.


科目:高中化学 来源: 题型:
【题目】根据要求完成下列问题
(1)写出 ![]() 中含有苯环的所有同分异构体
中含有苯环的所有同分异构体
(2)C7H5O2Cl的同分异构体中含有苯环且Cl直接和苯环相接能发生银镜反应的共有种,其中核磁共振氢谱有三种不同化学环境的氢,且峰面积比为2:2:1的是(写结构简式).
(3) 的一种同分异构体满足下列条件:
的一种同分异构体满足下列条件:
Ⅰ.能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应.
Ⅱ.分子中有6种不同化学环境的氢,且分子中含有两个苯环.
写出该同分异构体的结构简式:(写出一个就可以)
(4)某有机物X(C4H6O5)广泛存在于许多水果内,尤其以苹果、葡萄、西瓜、山楂为多.该化合物具有如下性质:①1molX与足量金属钠反应产生1.5mol气体;②在有浓H2SO4和加热条件下,X与醇或羧酸均反应生成有香味的产物;③X在一定条件下的分子内脱水产物(不是环状化合物)可和溴水发生加成反应.
根据上述信息,写出有机物X 可能的结构简式:(至少写出两种)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为A、B两种固体物质的溶解度随温度变化的曲线。请回答:
(1)30 ℃时,A、B两物质的溶解度________。
(2)20 ℃时,A物质的溶解度________B物质的溶解度(填“>”、“<”或“=”)。
(3)40 ℃时,将A、B各15 g分别加到均盛有50 g水的两只小烧杯中,充分搅拌后,________物质有剩余(填“A”或“B”)。

(4)现有50 ℃时A物质的不饱和溶液在不减少溶剂的情况下,欲使其变成饱和溶液,下列措施肯定不能实现的是________(填序号)。
①降低温度 ②升高温度 ③加入A物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是利用二氧化硅制备硅及其化合物的流程,下列说法正确的是( )
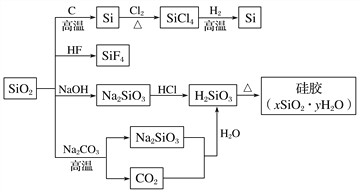
A. SiO2既能与HF反应,又能与NaOH反应,属于两性氧化物
B. Na2SiO3俗称水玻璃
C. 硅胶可用作袋装食品、瓶装药品干燥剂和催化剂的载体
D. 天然单质硅广泛用于制作光导纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】真空碳热还原-氯化法可实现由铝土矿制备金属铝。其核心步骤反应为:Al2O3+3Cl2+3C = 2AlCl3 + 3CO。对于该反应下列说法不正确的是( )
A.Al2O3 为氧化剂B.CO 为氧化产物C.AlCl3 为还原产物D.C 为还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随原子序数递增,八种短周期元素(用字母等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。

根据判断出的元素回答问题:
(1)f在周期表中的位置是___________。
(2)比较d、e常见离子的半径大小(用化学式表示,下同):______>_____;比较g、h的最高价氧化物对应水化物的酸性强弱:______>______。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由CO2、H2和CO组成的混合气体在同温同压下与氮气的密度相同。则该混合气体中CO2、H2和CO的体积比为( )
A.29∶8∶13B.22∶1∶14C.13∶16∶29D.26∶16∶57
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中能大量共存的是( )
A.K +、SiO32﹣、OH ﹣、Na +
B.Na +、H +、CO32﹣、SO42﹣
C.K +、H +、SiO32﹣、Cl ﹣
D.OH ﹣、Na +、HCO3﹣、Cl ﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com