
����Ŀ������ʵ����������������������������Ӧ����ȷ���ǣ� ��
���������� | ���� | |
A | ��ʢ��Ũ������Թ��м���ͭƬ��ͭƬ�ܿ쿪ʼ�ܽ⣬���ų��̼�����ζ������ | Ũ�������ǿ������ |
B | ����֧ʢ��KI3����Һ���Թ��У��ֱ�μӵ�����Һ����������Һ��ǰ����Һ�����������л�ɫ���� | KI3��Һ�д���ƽ�⣺I |
C | ��һ��������������Һ���ȵμ�KCl��Һ���ٵμ�KI��Һ���ȳ��ְ�ɫ����������ֻ�ɫ���� | Ksp(AgCl)��Ksp(AgI) |
D | �����£���pH��ֽ�ֱ�ⶨŨ��Ϊ0.1mol/LNaClO��Һ��0.1mol/LCH3COONa��Һ��pH | �Ƚ�HClO��CH3COOH������ǿ�� |
A.AB.BC.CD.D
���𰸡�B
��������
A��ͭ��Ũ����ķ�Ӧ��Ҫ���ȣ������£���������������������ȷ����A����
B������֧ʢ��KI3����Һ���Թ��У��ֱ�μӵ�����Һ����������Һ��ǰ����Һ������˵����Һ�д���I2�������л�ɫ������˵����Һ�д���I-��˵��KI3��Һ�д���ƽ�⣺I![]() I2+I-����B��ȷ��
I2+I-����B��ȷ��
C����һ��������������Һ���ȵμ�KCl��Һ���ٵμ�KI��Һ���ȳ��ְ�ɫ����������ֻ�ɫ��������������Ϊ��Һ����������������˲���˵��Ksp(AgCl)��Ksp(AgI)��ʵ����۲���ȷ����C����
D��NaClO��Һ����ǿ�����ԣ�������pH��ֽ�ⶨŨ��Ϊ0.1mol/LNaClO��Һ��pH��ʵ���������ȷ����D����
��ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
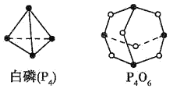
����Ŀ����1����ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ��̣���ѧ���ļ������γ�(���)1mol��ѧ��ʱ�ͷ�(������)����������֪����P4O6�ķ��ӽṹ��ͼ��ʾ�����ṩ���»�ѧ���ļ��ܣ�P-P��198kJ��mol-1��P-O��360 kJ��mol-1��O=O��498kJ��mol-1����ӦP4(����)��O2��Ӧ����P4O6���Ȼ�ѧ��Ӧ����ʽΪ____��
��2����(N2H4)����Ϊ�����������ȼ�ϣ���������N2O4��Ӧ����N2��ˮ��������֪��
��N2(g)��2O2(g)�TN2O4(l) ��H1�T-19.5kJ/mol
��N2H4(l)��O2(g)�TN2(g)��2H2O(g) ��H2�T-534.2kJ/mol
д���º�N2O4��Ӧ���Ȼ�ѧ����ʽ_____��
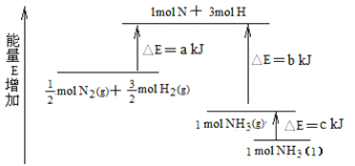
��3����ѧ��ӦN2��3H2![]() 2NH3�������仯��ͼ��ʾ���÷�Ӧ����NH3(l)���Ȼ�ѧ����ʽ��_____��
2NH3�������仯��ͼ��ʾ���÷�Ӧ����NH3(l)���Ȼ�ѧ����ʽ��_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ᱻ��Ϊ����������֮ĸ����ij��ѧ��ȤС���Ũ������ͭƬ�ķ�Ӧ����̽����������������⡣
(1)д����Ӧ�տ�ʼ�λ�ѧ����ʽ��������˫�����ű������ת�Ƶķ������Ŀ______________���ýη�Ӧ����Ϊ_________��
(2)����ͭ��ʣ�࣬��Ӧ��Ҫ����ʱ�����ӷ���ʽ��________������Ӧֹͣʱ���ټ���ϡ���ᣬ��ʱͭƬ���������ݲ�������ԭ����_______��
(3)���Թܽ���Ӧ������NO2�ռ�����������������ˮ�У����Թ���Һ�治������ʱ���Թ���ʣ����������ԼΪԭ���������________(��ͬ������)
(4)��12.8gͭ��һ��������Ũ���ᷴӦ��ͭ��ȫ�ܽ�ʱ������NO��NO2������干5.6L(��״��)����Ӧ��ת�Ƶĵ��ӵ����ʵ���Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.025molBaSO4��ĩ����ʢ������ˮ���ձ����γ�1L ����Һ��Ȼ�����ձ��м���Na2CO3����(������Һ����ı仯)����ֽ��衣����Na2CO3����Ĺ�������Һ�м������ӵ�Ũ�ȱ仯������ͼ��ʾ������˵������ȷ���ǣ� ��
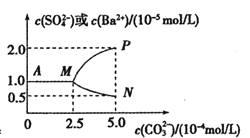
A.�����£�Ksp(BaSO4)=2.5��10-9
B.BaSO4�е��ܽ�ȡ�Ksp������BaCl2��Һ�еĴ�
C.��ҪʹBaSO4ȫ��ת��ΪBaCO3����Ҫ����0.65mol Na2CO3
D.BaSO4ǡ��ȫ��ת��ΪBaCO3ʱ����Һ������Ũ�ȴ�С��ϵΪ��c(![]() )>c(
)>c(![]() )>c(Ba2+)>c(OH-)
)>c(Ba2+)>c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijУ��ѧ�о�С����Զ�У���������������вⶨ��ش��������⡣
(1)����ͬѧ�������ͼ��ʾ��ʵ��װ�ã��Կ�����SO2�����������ﺬ�����вⶨ������װ�����ӵ�˳��Ϊ(����� )________________��
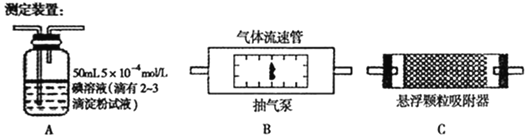
ע���������ٹ�������������λʱ����ͨ������������װ��
��������װ�ö����ⶨ�����е�SO2�Ϳ���������ĺ��������ⶨ��������(��λ��cm3��min-1)���Ҫ�ⶨ____________��____________��
����֪���ⵥ������ˮ��KI�����������ˮ�е��ܽ�ȡ�����Э������ͬѧ���100mL 5��10-4mo1 L-1����Һ�����ƣ�
��һ�����õ�����ƽȷ��ȡ1.27g�ⵥ�ʼ����ձ��У�______________��
�ڶ���������һ��������Һ��ϴ��Һȫ��ת��_____ mL������ƿ�У���ˮ���ݣ�ҡ�ȡ�
���������ӵڶ���������Һ��ȡ��10.00mL��Һ����100mL����ƿ�У���ˮϡ�����̶��ߣ�ҡ�ȡ�
(2)����ͬѧ������ͼ����װ�òⶨ�����е�SO2������

�ټ���װ�õ�������ʱ�������Թ���װ��������ˮ(��֤�����ܵ��¶˽�û��ˮ��)��Ȼ��__________(��д��������)ʱ�����ῴ��_____________(��дʵ������)����֤����װ�õ����������á�
�ڲⶨָ���ص�����е�SO2����ȷ��ȡ1.00mL 5��10-4mo1L-1����Һ��ע����ͼ��ʾ�Թ��С�������������ˮ�N�ͺ��ټ�2~3�ε�����Һ�����Ƴ���ҺA���ס�������ͬѧ�ֱ�ʹ����ͼ��ʾ��ͬ��ʵ��װ�ú���ҺA����ͬһ�ص㡢ͬʱ����ע�����Ļ���������������ֱ����Һ����ɫȫ���ʾ�Ϊֹֹͣ��������¼������������(����ÿ�γ���500mL)��
���� | ���� | ���� |
�������� | 110 | 145 |
�ҹ����������������Կ��������ⶨ��SO2�����Ũ����ֵ���±���
���Ũ����ֵ/mg��m-3 | ||
һ���� | ������ | ������ |
0.15 | 0.50 | 0. 70 |
����ʦ��ͬѧ�Ƿ������жϼ���ⶨ�����Ϊȷ����õص�Ŀ�����SO2 �ĺ���Ϊ_______mgm-3(����2 λ��Ч����)������________(���)�����������������ʵ���������ϴ�ƫ���ԭ����(����С������װ�ú�ҩƷ��������)______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ��������������ȷ����( )
A.���³�ѹ�£�32 g���������ԼΪ22.4L
B.1.8 g NH4+�к��е�������ΪNA
C.���³�ѹ�£�48g O3���е���ԭ����Ϊ3NA
D.2.4 g����þ��Ϊþ����ʱʧȥ�ĵ�����Ϊ0.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪101kPaʱ�������ȼ����Ϊ5518kJ/mol��ǿ����ǿ����ϡ��Һ�з�����Ӧʱ���к���Ϊ57.3kJ/mol���������Ȼ�ѧ����ʽ��д��ȷ����
��C8H18��l��+![]() O2��g��=8CO2��g��+9H2O��l������H=+5518kJ/mol��
O2��g��=8CO2��g��+9H2O��l������H=+5518kJ/mol��
��C8H18��l��+![]() O2��g��=8CO2��g��+9H2O��l������H=��5518kJ/mol��
O2��g��=8CO2��g��+9H2O��l������H=��5518kJ/mol��
��![]() H2SO4��aq��+Ba(OH) 2��aq��=
H2SO4��aq��+Ba(OH) 2��aq��=![]() BaSO4��s��+H2O��l������H=��57.3kJ/mol��
BaSO4��s��+H2O��l������H=��57.3kJ/mol��
��H+��aq��+OH����aq��=H2O��l������H=��57.3kJ/mol��
A.�٢�B.�ڢ�C.�ڢ�D.�ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڷ�Ӧ3Cl2��6KOH![]() KClO3��5KCl��3H2O������˵����ȷ����( )
KClO3��5KCl��3H2O������˵����ȷ����( )
A.Cl2����������KOH�ǻ�ԭ��
B.����������Ԫ�ص������DZ���ԭ����Ԫ��������5��
C.3 mol�����μӷ�Ӧת��6 mol����
D.KOH��KCl��KClO3 ���ǵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ɫ��ѧ����Ԥ����Ⱦ���ĸ����ֶΣ�����Ŀ�����о���Ѱ���ܳ�����õ�����ԭ���ϣ�����ȵؽ�Լ��Դ���ڻ����������������ж�ʵ�־���������Ⱦ��
��1�����и����������ɫ��ѧ��Ҫ�����____��
A������������ B��������Ⱦ�� C�������ж��� D���ž���ȾԴ
��2�����ҹ��������У�ij��Ϊ�ィһ���ͻ������أ����������з�������������Ϊ���е���____��
A�����������ɺ���������ƶ�¸�
B��Ӧ����ˮ��Դ�ḻ�ͽ�ͨ������Զ����еĽ���
C����ҵ��Ȩ����ѡ��ַ
D�����˽����˿ڳ��ܵľ�����
��3��ij�������ŷŵ���ˮ�к���Mg2+��Fe3+��Cu2+��Hg2+�������ӡ�ijͬѧ����˴Ӹ���ˮ�л��մ����Ľ���ͭ�ķ�����

�����Ƶô�ͭ�ķ����У���һ�������ᵼ�»�����Ⱦ��___��Ӧ������Щ��ʩ��ֹ��Ⱦ______��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com