
| A. | 乙醇与金属钠反应时,是乙醇分子中羟基中的O-H键断裂 | |
| B. | 检验乙醇中是否含有水,可加入少量无水硫酸铜,若变蓝则含水 | |
| C. | 禁止用工业酒精配制饮用酒和调味用的料酒 | |
| D. | 溴乙烷、TNT、丙三醇都是无色溶于水的有机化合物 |
分析 A.Na与乙醇反应生成氢气,O-H键断裂;
B.无水硫酸铜遇水变蓝;
C.工业酒精含有毒的甲醇;
D.溴乙烷、TNT均不溶于水.
解答 解:A.Na与乙醇反应生成氢气,乙醇分子中羟基中的O-H键断裂,故A正确;
B.无水硫酸铜遇水变蓝,则加入少量无水硫酸铜,若变蓝则含水,故B正确;
C.工业酒精含有毒的甲醇,则禁止用工业酒精配制饮用酒和调味用的料酒,故C正确;
D.溴乙烷、TNT均不溶于水,只有丙三醇是无色溶于水的有机化合物,故D错误;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的性质、有机反应、有机物组成等为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤族元素是典型的非金属元素,因此不能与其他非金属元素反应 | |
| B. | 碱金属元素单质越活泼,其熔点和沸点就越高 | |
| C. | 卤族元素单质都能和氢气反应,且气态氢化物的稳定性随单质氧化性的增强而增强 | |
| D. | 卤族元素单质都能与水剧烈反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ②③⑤ | C. | ①②⑤ | D. | ①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
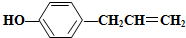 ,下列叙述不正确的是( )
,下列叙述不正确的是( )| A. | 1 mol胡椒粉最多可与4 mol氢气发生反应 | |
| B. | 1 mol胡椒粉最多可与3 mol溴水发生反应 | |
| C. | 胡椒粉可与氯化铁溶液反应,使溶液呈紫色 | |
| D. | 胡椒粉与NaHCO3溶液反应产生CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
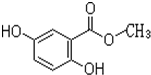 .
.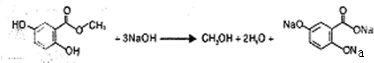 .
.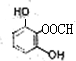 、
、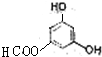 .
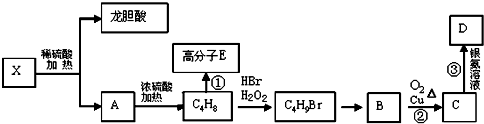
.
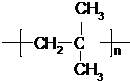 .
.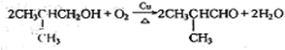 .
.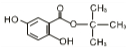 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在中和滴定实验中,锥形瓶用蒸馏水洗净后即可使用,滴定管用蒸馏水洗净后,须经干燥或润洗后方可使用 | |
| B. | 用碱式滴定管量取25.00mL高锰酸钾溶液 | |
| C. | 向冰醋酸中加水至配成醋酸稀溶液的过程中H+的浓度逐渐减小 | |
| D. | 25℃时NH4Cl溶液的KW大于100℃时NaCl溶液的KW |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com