
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| ① | | | | | | | | | | | | | | | | | |
| | ② | | | | | | | | | | | | ③ | ④ | ⑤ | ⑥ | |
| | ⑦ | | | | | | | | | | | | | | | ⑧ | |
| | | | | | ⑨ | | | | | ⑩ | | | | | | | |
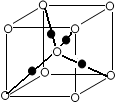
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
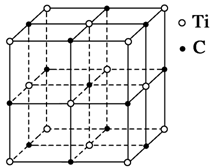
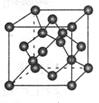
| A.Ti14C13 | B.TiC | C.Ti4C4 | D.Ti4C3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.由分子间作用力结合而成,熔点低 |
| B.固体或熔融后易导电,熔点在1000℃左右 |
| C.由共价键结合成网状结构,熔点高 |
| D.固体不导电,但溶于水或熔融后能导电 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.因纳米粒子半径太小,故不能将其制成胶体 |
| B.一定条件下纳米粒子可催化水的分解 |
| C.一定条件下,纳米陶瓷可发生任意弯曲,可塑性好 |
| D.纳米粒子半径小,表面活性高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
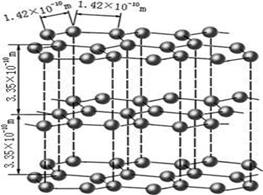
| A.晶体熔点由低到高:CF4<CCl4<CBr4<CI4 |
| B.硬度由大到小:金刚石>碳化硅>晶体硅 |
| C.熔点由高到低:Na>Mg>Al |
| D.晶格能由大到小:NaF> NaCl> NaBr>NaI |

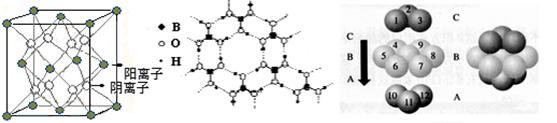
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com