

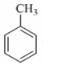
 ·Ö×ÓÖŠ²»Ķ¬»Æѧ»·¾³µÄĒāŌ×Ó¹²ÓŠ4ÖÖ£¬¹²ĆęŌ×ÓŹżÄæ×ī¶ąĪŖ13£®
·Ö×ÓÖŠ²»Ķ¬»Æѧ»·¾³µÄĒāŌ×Ó¹²ÓŠ4ÖÖ£¬¹²ĆęŌ×ÓŹżÄæ×ī¶ąĪŖ13£®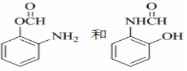 £®
£® £¬øĆ²½·“Ó¦µÄÖ÷ŅŖÄæµÄŹĒ±£»¤°±»ł£®
£¬øĆ²½·“Ó¦µÄÖ÷ŅŖÄæµÄŹĒ±£»¤°±»ł£®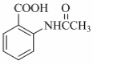 ĪŖÖ÷ŅŖŌĮĻ£¬¾×īÉŁ²½ÖčÖʱøŗ¬ėļü¾ŪŗĻĪļµÄĮ÷³Ģ£®
ĪŖÖ÷ŅŖŌĮĻ£¬¾×īÉŁ²½ÖčÖʱøŗ¬ėļü¾ŪŗĻĪļµÄĮ÷³Ģ£®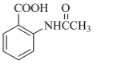 ”$”ś_{·“Ó¦Ģõ¼ž}^{·“Ó¦ŹŌ¼Į}$Äæ±ź»ÆŗĻĪļ ”$”ś_{·“Ó¦Ģõ¼ž}^{·“Ó¦ŹŌ¼Į}$Äæ±ź»ÆŗĻĪļ |
·ÖĪö £Ø1£©¼×±½ŗ¬ÓŠ1øö¼×»ł£¬±½»·×óÓŅ¶Ō³Ę£»±½»·ĪŖĘ½ĆęŠĪ½į¹¹£¬Óė±½»·Ö±½ÓĻąĮ¬µÄŌ×ÓŌŚĶ¬Ņ»øöĘ½ĆęÉĻ£»
£Ø2£©BĪŖĮŚĻõ»ł¼×±½£¬¶ŌÓ¦µÄĶ¬·ÖŅģ¹¹Ģå£ŗa£®±½»·ÉĻÖ»ÓŠĮ½øöČ”“ś»łĒŅ»„ĪŖĮŚĪ»£¬b£®¼ČÄÜ·¢ÉśŅų¾µ·“Ó¦ÓÖÄÜ·¢ÉśĖ®½ā·“Ó¦£¬ĖµĆ÷Ó¦ŗ¬ÓŠõ„»ł£¬ĒŅĪŖ¼×Ėįõ„£¬ĮķĶāŅ»ÖÖ¹ŁÄÜĶÅĪŖ°±»ł£»
£Ø3£©Čē²ÉÓĆ¼×±½Ö±½ÓĻõ»ÆµÄ·½·ØÖʱøB£¬Ļõ»łæÉČ”“ś¼×»ł¶ŌĪ»µÄHŌ×Ó£»
£Ø4£©Óɽį¹¹¼ņŹ½æÉÖŖ·“Ó¦¢ŽĪŖČ”“ś·“Ó¦£¬æɱÜĆā°±»ł±»Ńõ»Æ£»
£Ø5£©¢ąĪŖ±½»·µÄĀČ“ś·“Ó¦£¬Ó¦ŌŚĄąĖʱ½ÓėäåµÄ·“Ó¦£»Fŗ¬ÓŠōČ»ł”¢°±»łŗĶĀČŌ×Ó£»
£Ø6£© æÉĖ®½āÉś³É
æÉĖ®½āÉś³É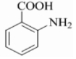 £¬ŗ¬ÓŠ°±»ł”¢ōČ»ł£¬æÉ·¢ÉśĖõ¾Ū·“Ӧɜ³Éøß¾ŪĪļ£®
£¬ŗ¬ÓŠ°±»ł”¢ōČ»ł£¬æÉ·¢ÉśĖõ¾Ū·“Ӧɜ³Éøß¾ŪĪļ£®
½ā“š ½ā£ŗ£Ø1£©¼×±½ŗ¬ÓŠ1øö¼×»ł£¬±½»·×óÓŅ¶Ō³Ę£¬Ōņ·Ö×ÓÖŠ²»Ķ¬»Æѧ»·¾³µÄĒāŌ×Ó¹²ÓŠ4ÖÖ£¬±½»·ĪŖĘ½ĆęŠĪ½į¹¹£¬Óė±½»·Ö±½ÓĻąĮ¬µÄŌ×ÓŌŚĶ¬Ņ»øöĘ½ĆęÉĻ£¬½įŗĻČżµćČ·¶ØŅ»øöĘ½Ćę£¬¼×»łÉĻæÉÓŠ1øöHÓė±½»·¹²Ę½Ćę£¬¹²13øö£¬
¹Ź“š°øĪŖ£ŗ4£» 13£»
£Ø2£©BĪŖ2-Ļõ»ł¼×±½»ņĮŚĻõ»ł¼×±½£¬¶ŌÓ¦µÄĶ¬·ÖŅģ¹¹Ģå£ŗa£®±½»·ÉĻÖ»ÓŠĮ½øöČ”“ś»łĒŅ»„ĪŖĮŚĪ»£¬b£®¼ČÄÜ·¢ÉśŅų¾µ·“Ó¦ÓÖÄÜ·¢ÉśĖ®½ā·“Ó¦£¬ĖµĆ÷Ó¦ŗ¬ÓŠõ„»ł£¬ĒŅĪŖ¼×Ėįõ„£¬ĮķĶāŅ»ÖÖ¹ŁÄÜĶÅĪŖ°±»ł£¬æÉÄÜĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ2-Ļõ»ł¼×±½»ņĮŚĻõ»ł¼×±½£» £»
£»
£Ø3£©Čē²ÉÓĆ¼×±½Ö±½ÓĻõ»ÆµÄ·½·ØÖʱøB£¬Ļõ»łæÉČ”“ś¼×»ł¶ŌĪ»µÄHŌ×Ó£¬ÄæµÄŹĒ±ÜĆā±½»·ÉĻ¼×»ł¶ŌĪ»µÄĒāŌ×Ó±»Ļõ»łČ”“ś£¬
¹Ź“š°øĪŖ£ŗ±ÜĆā±½»·ÉĻ¼×»ł¶ŌĪ»µÄĒāŌ×Ó±»Ļõ»łČ”“ś£»
£Ø4£©Óɽį¹¹¼ņŹ½æÉÖŖ·“Ó¦¢ŽĪŖČ”“ś·“Ó¦£¬·“Ó¦µÄ·½³ĢŹ½ĪŖ £¬øĆ²½·“Ó¦µÄÖ÷ŅŖÄæµÄŹĒ±ÜĆā°±»ł±»Ńõ»Æ£¬
£¬øĆ²½·“Ó¦µÄÖ÷ŅŖÄæµÄŹĒ±ÜĆā°±»ł±»Ńõ»Æ£¬
¹Ź“š°øĪŖ£ŗ £»±£»¤°±»ł£»
£»±£»¤°±»ł£»
£Ø5£©¢ąĪŖ±½»·µÄĀČ“ś·“Ó¦£¬Ó¦ŌŚĄąĖʱ½ÓėäåµÄ·“Ó¦£¬·“Ó¦Ģõ¼žĪŖCl2/FeCl3£Ø»ņCl2/Fe£©£¬FÖŠŗ¬Ńõ¹ŁÄÜĶŵÄĆū³ĘĪŖōČ»ł£¬
¹Ź“š°øĪŖ£ŗCl2/FeCl3£Ø»ņCl2/Fe£©£»ōČ»ł£»
£Ø6£© æÉĖ®½āÉś³É
æÉĖ®½āÉś³É £¬ŗ¬ÓŠ°±»ł”¢ōČ»ł£¬æÉ·¢ÉśĖõ¾Ū·“Ӧɜ³Éøß¾ŪĪļ£¬·“Ó¦µÄĮ÷³ĢĪŖ
£¬ŗ¬ÓŠ°±»ł”¢ōČ»ł£¬æÉ·¢ÉśĖõ¾Ū·“Ӧɜ³Éøß¾ŪĪļ£¬·“Ó¦µÄĮ÷³ĢĪŖ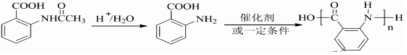 £¬
£¬
¹Ź“š°øĪŖ£ŗ £®
£®
µćĘĄ ±¾ĢāĪŖ2017ÄźĢģ½ņæ¼Ģā£¬ĪŖÓŠ»śĪļŗĻ³ÉĢāÄ棬²ąÖŲæ¼²éѧɜ·ÖĪöÅŠ¶ĻÄÜĮ¦£¬Ć÷Č·¹ŁÄÜĶż°ĘäŠŌÖŹ¹ŲĻµ”¢³£¼ū·“Ó¦ĄąŠĶ¼°·“Ó¦Ģõ¼žŹĒ½ā±¾Ģā¹Ų¼ü£¬×¢ŅāĢāøųŠÅĻ¢µÄĮé»īŌĖÓĆ£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1L0.1mol•L-1NH4ClČÜŅŗÖŠ£¬NH4+µÄŹżĮæĪŖ0.1NA | |
| B£® | 2.4gMgÓėH2SO4ĶźČ«·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ0.1NA | |
| C£® | ±ź×¼×“æöĻĀ£¬2.24LN2ŗĶO2µÄ»ģŗĻĘųĢåÖŠ·Ö×ÓŹżĪŖ0.2NA | |
| D£® | 0.1mol H2ŗĶ0.1mol I2ÓŚĆܱÕČŻĘ÷ÖŠ³ä·Ö·“Ó¦ŗó£¬Ęä·Ö×Ó×ÜŹżĪŖ0.2NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 Č«¹ĢĢ¬ļ®Įņµē³ŲÄÜĮæĆܶČøß”¢³É±¾µĶ£¬Ę乤×÷ŌĄķČēĶ¼ĖłŹ¾£¬ĘäÖŠµē¼«a³£ÓĆ²ōÓŠŹÆÄ«Ļ©µÄS8²ÄĮĻ£¬µē³Ų·“Ó¦ĪŖ£ŗ16Li+xS8=8Li2Sx£Ø2”Üx”Ü8£©£®ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©
Č«¹ĢĢ¬ļ®Įņµē³ŲÄÜĮæĆܶČøß”¢³É±¾µĶ£¬Ę乤×÷ŌĄķČēĶ¼ĖłŹ¾£¬ĘäÖŠµē¼«a³£ÓĆ²ōÓŠŹÆÄ«Ļ©µÄS8²ÄĮĻ£¬µē³Ų·“Ó¦ĪŖ£ŗ16Li+xS8=8Li2Sx£Ø2”Üx”Ü8£©£®ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©| A£® | µē³Ų¹¤×÷Ź±£¬Õż¼«æÉ·¢Éś·“Ó¦£ŗ2Li2S6+2Li++2e-=3Li2S4 | |
| B£® | µē³Ų¹¤×÷Ź±£¬ĶāµēĀ·ÖŠĮ÷¹ż0.02 molµē×Ó£¬øŗ¼«²ÄĮĻ¼õÖŲ0.14 g | |
| C£® | ŹÆÄ«Ļ©µÄ×÷ÓĆÖ÷ŅŖŹĒĢįøßµē¼«aµÄµ¼µēŠŌ | |
| D£® | µē³Ų³äµēŹ±¼äŌ½³¤£¬µē³ŲÖŠµÄLi2S2ĮæŌ½¶ą |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.1mol•L-1µÄNH4ClČÜŅŗÖŠŗ¬NH4+µÄŹżÄæŠ”ÓŚ0.01NA | |
| B£® | øĆ·“Ó¦ŹĶ·ÅH2µÄ·Ö×ÓŹżĪŖ$\frac{V}{22.4}$NA | |
| C£® | ·“Ó¦ÖŠĆæĻūŗÄ2molH+×ŖŅʵĵē×ÓŹżĪŖ6NA | |
| D£® | 120.5gNCl3ÖŠĖłŗ¬¹²¼Ū¼üŹżĪŖ4NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na2O2ĪüŹÕCO2²śÉśO2£¬æÉÓĆ×÷ŗōĪüĆę¾ß¹©Ńõ¼Į | |
| B£® | ClO2¾ßÓŠ»¹ŌŠŌ£¬æÉÓĆÓŚ×ŌĄ“Ė®µÄɱ¾śĻū¶¾ | |
| C£® | SiO2Ó²¶Č“ó£¬æÉÓĆÓŚÖĘŌģ¹āµ¼ĻĖĪ¬ | |
| D£® | NH3Ņ×ČÜÓŚĖ®£¬æÉÓĆ×÷ÖĘĄä¼Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ÅØ¶Č¾łĪŖ0.1 mol•L-1µÄ HCOONaŗĶNH4Cl ČÜŅŗÖŠŃōĄė×ÓµÄĪļÖŹµÄĮæÅضČÖ®ŗĶ£ŗĒ°Õß“óÓŚŗóÕß | |
| B£® | ÓĆĻąĶ¬ÅØ¶ČµÄNaOHČÜŅŗ·Ö±šµĪ¶ØµČĢå»żpH¾łĪŖ3µÄHCOOHŗĶCH3COOHČÜŅŗÖĮÖÕµć£¬ĻūŗÄNaOHČÜŅŗµÄĢå»żĻąµČ | |
| C£® | 0.2 mol•L-1 HCOOH Óė 0.1 mol•L-1 NaOH µČĢå»ż»ģŗĻŗóµÄČÜŅŗÖŠ£ŗc£ØHCOO-£©+c£ØOH-£©=c£ØHCOOH£©+c£ØH+£© | |
| D£® | 0.2 mol•L-1 CH3COONa Óė 0.1 mol•L-1ŃĪĖįµČĢå»ż»ģŗĻŗóµÄČÜŅŗÖŠ£ØpH£¼7£©£ŗc£ØCH3COO-£©£¾c£ØCl-£©£¾c£ØCH3COOH£©£¾c£ØH+£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | HOCH2CH=CH2ÄÜ·¢ÉśČ”“ś·“Ó¦£¬¼Ó³É·“Ó¦”¢Ńõ»Æ·“Ó¦ | |
| B£® | ŌĀ¹šĻ©£Ø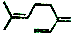 £©ĖłÓŠĢ¼Ō×ÓŅ»¶ØŌŚĶ¬Ņ»Ę½ĆęÉĻ £©ĖłÓŠĢ¼Ō×ÓŅ»¶ØŌŚĶ¬Ņ»Ę½ĆęÉĻ | |
| C£® | ¼×Ķ锢ŅŅĻ©”¢±½ŗĶŅŅ“¼¶¼ÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ« | |
| D£® | ÓĶÖ¬Ōķ»Æ·“Ó¦µĆµ½øß¼¶Ö¬·¾ĖįÓėøŹÓĶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
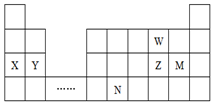
| A£® | Ō×Ó°ė¾¶£ŗY£¾Z£¾W£¬¼ņµ„Ąė×Ó°ė¾¶£ŗM-£¾Z2-£¾W2- | |
| B£® | µ„ÖŹµÄ»¹ŌŠŌ£ŗX£¾Y£¬¼ņµ„Ēā»ÆĪļµÄ·Šµć£ŗZ£¾W | |
| C£® | äåÓėŌŖĖŲMĶ¬Ö÷×壬×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄĖįŠŌ±ČMµÄĒæ | |
| D£® | ŌŖĖŲNĪ»ÓŚ½šŹōÓė·Ē½šŹōµÄ·Ö½ēĻßø½½ü£¬æÉŅŌĶʶĻNµÄµ„ÖŹæÉ×÷ °ėµ¼Ģå²ÄĮĻ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com