
分析 (1)根据n=$\frac{m}{M}$,V=n•Vm计算;
(2)1L水的质量为1000g,溶质的质量分数ω=$\frac{{m}_{溶质}}{{m}_{溶质}+{m}_{溶剂}}$×100%;
(3)由(1)得该气体在标准状况下的体积为$\frac{22.4m}{M}$L,带入$ρ=\frac{m}{V}$计算.
解答 解:(1)mg该气体的物质的量n=$\frac{m}{M}$=$\frac{mg}{Mg•mo{l}^{-1}}$=$\frac{m}{M}$mol,该气体在标准状况下的体积V=n•Vm=$\frac{m}{M}$mol×22.4L/mol=$\frac{22.4m}{M}$L,
故答案为:$\frac{22.4m}{M}$;
(2)1L水的质量为1000g,溶质的质量分数ω=$\frac{{m}_{溶质}}{{m}_{溶质}+{m}_{溶剂}}$×100%=$\frac{mg}{(1000+m)g}$×100%=$\frac{100m}{1000+m}$%,
故答案为:$\frac{100m}{1000+m}$%;
(3)由(1)得该气体在标准状况下的体积为$\frac{22.4m}{M}$L,$ρ=\frac{m}{V}$=$\frac{mg}{\frac{22.4m}{M}L}$=$\frac{M}{22.4}$g•L-1.
故答案为:$\frac{M}{22.4}$.
点评 本题考查物质的量的相关计算,题目难度中等,综合性较强,充分考查学生的分析、理解能力及灵活应用公式的能力.


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6.75 g | B. | 4.05g | C. | 2.70 g | D. | 1.80 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烷烃 | B. | 烯烃 | C. | 炔烃 | D. | 芳香烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
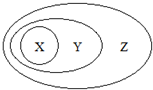 如图用交叉分类法表示了一些物质或概念之间的从属或包含关系,不正确的是( )
如图用交叉分类法表示了一些物质或概念之间的从属或包含关系,不正确的是( )| X | Y | Z | |
| A | CuSO4•5H2O | 盐 | 纯净物 |
| B | 胶体 | 分散系 | 混合物 |
| C | 碱性氧化物 | 氧化物 | 化合物 |
| D | 置换反应 | 氧化还原反应 | 离子反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 化学反应 | 离子方程式 | 评价 |
| A | Cu和AgNO3溶液反应 | Cu+Ag+═Cu2++Ag | 正确 |
| B | 氧化铝与NaOH溶液反应 | 2Al3++3O2-+2OH-═2AlO2-+H2O | 错误,Al2O3不应写成离子形式 |
| C | Fe和稀硫酸反应 | 2Fe+6H+═2Fe3++3H2↑ | 正确 |
| D | 钠与硫酸铜溶液反应 | 2Na+Cu2+═Cu+2Na+ | 错误,CuSO4不应写成离子形式 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
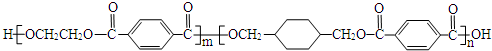
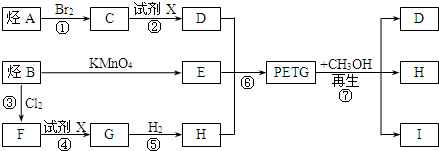
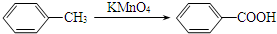
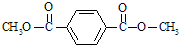 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 X、Y、Z、W 均为中学化学中常见物质或其溶液,一定条件下它们之间有如下转化关系(其它产物已略去),下列说法不正确的是( )
X、Y、Z、W 均为中学化学中常见物质或其溶液,一定条件下它们之间有如下转化关系(其它产物已略去),下列说法不正确的是( )| A. | 若 W 是单质铁,则 Z 溶液可能是 FeCl2 溶液 | |
| B. | 若 X 是碳酸钠,则 W 可能是盐酸 | |
| C. | 若 W 是氢氧化钠,则 X 与 Z 可反应生成 Y | |
| D. | 若 W 为氧气,则 Z 与水反应(或溶于水)一定生成一种强酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com