
| A. | 向稀盐酸中加NaNO3溶液 | B. | 向稀盐酸中加碳酸钠固体 | ||
| C. | 将锌粒制成薄片 | D. | 向稀盐酸中加食盐水 |
分析 产生氢气的量不变,则保证盐酸完全和金属反应生成氢气;加快反应速率,应增大盐酸的浓度和升高温度.
解答 解:A.向稀盐酸中加入硝酸钠溶液,相当于含有硝酸,硝酸和Zn反应生成氮氧化物而不是氢气,导致生成氢气的总量减少,故A错误;
B.加入碳酸钠固体,碳酸钠和稀盐酸反应生成二氧化碳,导致生成氢气总量减少,故B错误;
C.将锌粒制成薄片,增大反应物接触面积,加快反应速率,故C错误;
D.向稀盐酸中加入食盐水,导致氢离子浓度减小但氢离子总物质的量不变,则化学反应速率降低,但生成氢气总量不变,故D正确;
故选D.
点评 本题考查了影响反应速率的因素,为高频考点,侧重考查学生分析判断能力,注意题干中限制性条件“反应速率改变但生成氢气总量不变”,题目难度不大.


科目:高中化学 来源: 题型:实验题
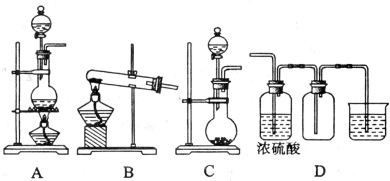
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ;
; ;A、B、E形成的化合物
;A、B、E形成的化合物 ;D、E形成的化合物
;D、E形成的化合物 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ②③ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 因SiO2不溶于水,故H2SiO3不是SiO2对应的酸,或者说SiO2不是H2SiO3的酸酐 | |
| B. | CO2通入水玻璃(Na2SiO3溶液)可以得到硅酸 | |
| C. | 因为高温时SiO2与Na2SiO3反应生成CO2,故硅酸的酸性比碳酸强 | |
| D. | 因为NH3•H2O是弱碱,所以不能用氨水与FeCl3溶液反应制取Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 粒子代码 | a | I | e |
| 原子核数 | 单核 | 四核 | 二核 |
| 粒子的电荷数 | 一个单位正电荷 | 0 | 一个单位负电荷 |

 .;
.; .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com