
有Al、CuO、Fe2O3组成的混合物共10.0 g,放入500 mL某浓度的盐酸溶液中,混合物完全溶解,当再加入250 mL 2.0 mol/L的NaOH溶液时,得到的沉淀最多,上述盐酸溶液的浓度为( )
A.0.5 mol/L B.1.0 mol/L
C.2.0 mol/L D.3.0 mol/L
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.化学变化过程是原子的重新组合过程
B.根据化学反应中的能量变化情况,化学反应可分为吸热反应和放热反应
C.化学反应中的能量变化多少与其反应物用量有关
D.化学反应中的能量变化都是以热能形式表现出来的
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.铜的化学性质活泼,不宜用铜制作盛食品的器皿
B.盛放NaOH溶液的玻璃试剂瓶不能用玻璃塞
C.只用KSCN溶液就可检验FeCl3溶液中的少量Fe2+
D.普通玻璃的组成可用Na2O·CaO·6SiO2表示,是纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应广泛应用于金属的冶炼。下列说法不正确的是( )
A.电解熔融氯化钠制取金属钠的反应中,钠离子被还原,氯离子被氧化
B.湿法炼铜与火法炼铜的反应中,铜元素都发生还原反应
C.用磁铁矿炼铁的反应中,1 mol Fe3O4被CO还原成Fe,转移9 mol e-
D.铝热法还原铁的反应中,放出的热量能使铁熔化
查看答案和解析>>
科目:高中化学 来源: 题型:
铁的氧化物有多种用途。请解答下面有关问题:
(1)赤铁矿的主要成分是Fe2O3,是工业炼铁的主要原料之一。写出由Fe2O3制得单质铁的化学方程式__________________________________。某赤铁矿除了含Fe2O3之外,还含有少量的SiO2和Al2O3。将试样溶于NaOH溶液,充分反应后过滤,即可得到较纯净的Fe2O3。发生反应的离子方程式是______________________________________________________________。
(2)Fe2O3可以与铝粉组成铝热剂用于焊接钢轨或定向爆破。某同学猜测,该反应所得熔融物中含有Fe2O3。他设计如下实验来验证自己的猜想:取少量试样,加入足量稀盐酸,然后滴加KSCN溶液,若出现红色,证明含有Fe2O3。否则,不含有Fe2O3。你认为该方案合理吗?为什么?__________________________________ __________________________________。
(3)合成氨工业中所用的α-Fe催化剂的主要成分是FeO、Fe2O3。已知当催化剂中Fe2+和Fe3+的物质的量之比为12时,其催化活性最高。某化学小组试图以Fe2O3为原料制备该催化剂,方法之一是向其中加入炭粉高温反应:2Fe2O3+C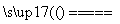 4FeO+CO2↑。
4FeO+CO2↑。
实验教师提供了12 g炭粉。请你计算,若要制取这种活性最高的催化剂,加入的Fe2O3的质量为________ g。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知乙炔与苯蒸气完全燃烧的热化学方程式如下:
①C2H2(g)+5/2O2(g)—→2CO2(g)+H2O(l) ΔH=-1 300 kJ/mol
②C6H6(g)+15/2O2(g)—→6CO2(g)+3H2O(l) ΔH=-3 295 kJ/mol
下列说法正确的是( )
A.1 mol C2H2(g)完全燃烧生成气态水时放热大于1 300 kJ
B.1 mol C6H6(l)完全燃烧生成液态水时放热大于3 295 kJ
C.相同条件下,等质量的C2H2(g)与C6H6(g)完全燃烧,C6H6(g)放热更多
D.C2H2(g)三聚生成C6H6(g)的过程属于放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列分子或离子在指定条件的分散系中能大量共存的是
A. Ca(NO3) 2溶液中: Fe2+、H+、Cl—、SO42—;
B.使pH试纸变蓝的溶液中:K+、NH4+、S-、SO32-;
C.水电离出的c(H+)=10-12 mol·L-1的溶液中:Na+、Ba2+、HCO3—、CH3COO-[;
D.透明的强酸性溶液中: Al3+、Fe3+、Cl-、SO42
查看答案和解析>>
科目:高中化学 来源: 题型:
物质A经下图所示的过程转化为含氧酸D,D为强酸,请回答下列问题:
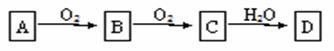
(1)若A在常温下为气体单质则回答:
①A、C的化学式分别是:A________;C________。
②将C通入水溶液中,反应化学方程式为_____________________________________________。
(2)若仅A、B在常温下为气体且为化合物, 则回答:
①A的化学式是:A_____________。
②B生成C的化学方程式为________________________________________________________。
③一定条件下碳单质与D反应的化学方程式为________________________________________,该反应中D起到的作用是__________性。
(3)若A在常温下为固体单质则回答:
①D的化学式是___________;
②向含2mol D的浓溶液中加入足量的Cu加热,标准状况下产生的气体体积_______22.4L(填“大于”“等于”或“小于”),原因为_______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com