
下列各组在溶液中的反应,不管反应物的量是多少,都能用同一离子方程式表示的是(  )
)
A.FeBr2与Cl2 B.Ba(OH)2与H2SO4
C.HCl与Na2CO3 D.NaHCO3与Ca(OH)2
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年天津市武清区等五区县高二上期中化学卷(解析版) 题型:选择题
下列说法正确的是
A.强电解质溶液的导电能力一定比弱电解质溶液的强
B.氨气是弱电解质,铜是强电解质
C.氢氧化钠是强电解质,醋酸是弱电解质
D.硫酸钠是强电解质,硫酸钡是弱电解质
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市河东区高二上学期期中质检化学试卷(解析版) 题型:选择题
25 ℃和1.01×105 Pa时,反应2N2O5(g)=4NO2(g)+O2(g) ΔH=+56.76 kJ/mol自发进行的原因是
A.是吸热反应 B.是放热反应
C.是熵减小的反应 D.熵增大效应大于能量效应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市河东区高二上学期期中质检化学试卷(解析版) 题型:选择题
化学与人类生活、社会可持续发展密切相关。下列措施有利于节能减排、保护环境的是
①加快化石燃料的开采与使用 ②研发易降解的生物农药 ③应用高效洁净的能源转化技术 ④田间焚烧秸秆 ⑤推广使用节能环保材料
A.①③⑤ B.②③⑤ C.①②④ D.②④⑤
查看答案和解析>>
科目:高中化学 来源:2017届贵州省高三上月考三化学试卷(解析版) 题型:填空题
Ⅰ.请回答:
(1)Na2O2的电子式 。
(2)除去FeCl3中少量FeCl2,除杂过程涉及的化学反应方程式 。
(3)往饱和Na2CO3溶液中通入CO2气体,溶液中出现白色浑浊,写出该反应的离子方程式 。
(4)双氧水能使酸性高锰酸钾溶液褪色,请完成以下相关反应的离子方程式:
( )MnO4-+( )H2O2+ =( )Mn2++( )H2O+ 。
Ⅱ.无机化合物A 和NaH都是重要的还原剂,遇水都强烈反应。一定条件下,2.40g NaH与气体B反应生成3.90g化合物A和 2.24L(已折算成标准状况)的H2。已知气体B可使湿润红色石蕊试纸变蓝。已知:NH3+ NH3=NH4++NH2-
请回答下列问题:
(1)A的化学式是 。
(2)A与足量盐酸发生非氧化还原反应的化学方程式 。
(3)在高温下氢化钠(NaH)可将四氯化钛(TiC14)还原成金属钛,该反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古高三上学期期中化学试卷(解析版) 题型:实验题
为探究碳铁合金与浓硫酸在酸性条件下反应的部分产物并测定碳铁合金中铁元素的质量分数,某化学小组设计了下图所示的实验装置,并完成以下实验探究。
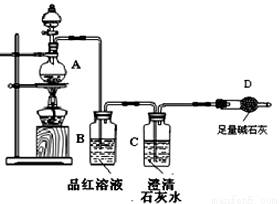
(1)往圆底烧瓶中加入m g铁碳合金,并滴入过量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:①常温下,Fe在浓硫酸中 ;②常温下,碳和浓硫酸不反应。
(2)装置B的作用是 。
(3)甲同学观察到装置C中有白色沉淀生成,他得出了使澄清石灰水变浑浊的气体是二氧化碳。装置A中能产生二氧化碳的化学方程式为 。
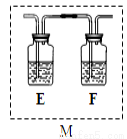
(4)乙同学认为甲同学的结论是错误的,他认为为了确认二氧化碳的存在,需在装置B-C之间添加装置M。装置E、F中盛放的试剂分别是酸性高锰酸钾、 。重新实验后 观察到装置F中的现象是 。
观察到装置F中的现象是 。
(5)有些同学认为合金中铁元素的质量分数可用KMnO4溶液来测定。
(5Fe2++MnO4—+8H+==5Fe3++Mn2++4H2O)。
测定铁元素质量分数的实验步骤如下:
I.往烧瓶A中加入过量的还原剂铜使溶液中的Fe3+完全转化为Fe2+,过滤,得到滤液B;
II.将滤液B稀释为250 mL;
III.取稀释液25.00 mL,用浓度为c mol·L—1的酸性KMnO4溶液滴定,三次滴定实验所需KMnO4溶液体积的平均值为V mL。
①步骤 Ⅱ中,将滤液B稀释为250 mL需要用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还必须要用到的是 ;
Ⅱ中,将滤液B稀释为250 mL需要用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还必须要用到的是 ;
②滴定过程中 (填“需要”或“不需要”)加入指示剂
③铁碳合金中铁元素的质量分数为 。
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古高三上学期期中化学试卷(解析版) 题型:选择题
镁铝合金5.1 g溶于300 ml 2mol/L的盐酸中,标准状况下,放出气体的体积为5.6 L,向反应后的溶液中加入500 ml NaOH溶液,充分反应后,最终产生白色沉淀。
下列有关说法不正确的是( )
A、5.1 g镁铝合金中含有镁和铝的质量分别为2.4g、2.7g
B、若白色沉淀只有Mg(OH)2,该NaOH溶液的浓度至少为1.2mol/L
C、生成沉淀的最大质量为13.6 g
D、溶解5.1 g镁铝合金时,剩余盐酸的物质的量为 0.1 mol
0.1 mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学卷(解析版) 题型:填空题
(1)家用液化石油气的主要成分之一是甲烷,当16 kg甲烷完全燃烧并生成二氧化碳气体和液态水时,放出的热量为8.9×105 kJ。已知1mol液态水汽化时需要吸收44 kJ热量。试写出甲烷燃烧生成水蒸气的热化学方程式: 。
(2)有同学用甲烷与空气为原料制作一燃烧电池,若以稀硫酸为电解质溶液时,其负极反应式为 。
(3)已知拆开1 mol H-H键,1 molN-H键,1 molN≡N键分别需要的能量是akJ、bkJ、ckJ,则N2与H2反应生成NH3的热化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高二上期中化学卷(解析版) 题型:选择题
恒 容容器中,2SO2(g) + O2(g)
容容器中,2SO2(g) + O2(g) 2SO3 (g) △H=—296.6kJ/mol,下列判断不正确的是( )
2SO3 (g) △H=—296.6kJ/mol,下列判断不正确的是( )
A.2体积SO2和足量O2反应,一定不能生成2体积SO3
B.其他条件不变,增大压强,正反应速率增大逆反应速率也增大
C.加入2molSO2和1molO2放出的热量是加入1molSO2和0.5molO2放出热量的2倍
D.在该容器中先投入1molSO3,平衡后再加入1molSO3,达新平衡后SO2的体积分数比原平衡减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com