
| A. | X的分子式为C5H10O2 | |
| B. | X可能的结构有两种 | |
| C. | Y中含有的官能团有羧基和碳碳双键 | |
| D. | X与Y相对分子质量相差14,则X与Y互为同系物 |
分析 该反应为合成甲基丙烯酸甲酯的反应,CH3C≡CH、CO、CH3OH在一定条件下反应生成X,为加成反应,X可水解,应属于酯类,X应为CH2=C(CH3)COOCH3,则Y为CH2=C(CH3)COOH,以此解答该题.
解答 解:A.X应为CH2=C(CH3)COOCH3,分子式为C5H8O2,故A错误;
B.X为CH2=C(CH3)COOCH3,结构有1种,故B错误;
C.Y为CH2=C(CH3)COOH,含有羧基和碳碳双键,故C正确;
D.X为CH2=C(CH3)COOCH3,则Y为CH2=C(CH3)COOH,二者不是同系物,故D错误.
故选C.
点评 本题考查有机物的合成,为高频考点,侧重考查学生的分析能力,注意把握有机物的性质以及题给信息,难度不大.


 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 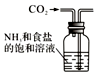 装置可用于模拟侯氏制碱法制取碳酸氢钠 | |
| B. | 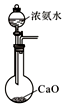 装置可用于制备少量NH3 | |
| C. |  装置可用于准确量取一定体积K2Cr2O7标准溶液 | |
| D. | 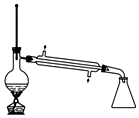 装置常用于分离互不相溶的液体混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
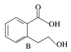 )的同分异构体的数目有4个;写出其中任意一个同分异构体的结构简式:
)的同分异构体的数目有4个;写出其中任意一个同分异构体的结构简式: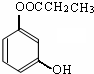 (或
(或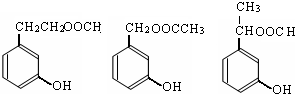 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
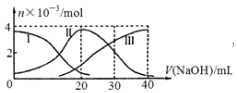 手持技术是基于数据采集器、传感器和多媒体计算机构成的一种新兴掌上试验系统,具有实时、定量、直观等特点,如图是利用手持技术得到的微粒的物质的量的变化图,常温下向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液,其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-,下列说法正确的是( )
手持技术是基于数据采集器、传感器和多媒体计算机构成的一种新兴掌上试验系统,具有实时、定量、直观等特点,如图是利用手持技术得到的微粒的物质的量的变化图,常温下向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液,其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-,下列说法正确的是( )| A. | H2A在水中的电离方程式是:H2A═2H++A2- | |
| B. | 当V(NaOH)=40mL时,其溶液中水的电离受到抑制 | |
| C. | 当V(NaOH)=20mL时,则有:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) | |
| D. | 当V(NaOH)=30mL时,则有:c(H+)+c(Na+)═c(A2-)+c(OH-)+c(HA-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氮氧化物是造成雾霾天气的主要原因之一,消除氮氧化物有多种方法.
氮氧化物是造成雾霾天气的主要原因之一,消除氮氧化物有多种方法.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
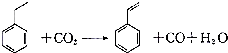 ,下列有关说法正确的是( )
,下列有关说法正确的是( )| A. | 苯乙烯分子中含有4个碳碳双键 | B. | 苯乙烯分子式为C8H10 | ||
| C. | 乙苯有三种同分异构体 | D. | 乙苯能发生取代、加成和氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com