
【题目】盐酸普鲁卡因[H2N![]() COOCH2CH2N+H(C2H5)2·Cl-]是一种麻醉药,可由乙烯和苯合成。流程如下:
COOCH2CH2N+H(C2H5)2·Cl-]是一种麻醉药,可由乙烯和苯合成。流程如下:
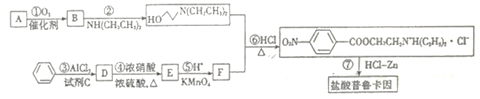
已知: I.B核磁共振氢谱只有1组峰; D的相对分子质量为92。
II.试剂C 是一氯代烃,与苯的反应为: ![]()
回答下列问题:
(1)F的结构简式为______________,它含有的官能团名称是_____________________。
(2)反应④的反应类型为______反应,其化学方程式:___________________________。
(3)反应③的化学方程式为______________________________________。
(4)E的既能发生银镜反应,又能遇FeCl3溶液显色且不含酰胺键的芳香族同分异构体有____种,任写其一种结构简式:________________________________。
(5)参照上述合成路线,设计由甲苯合成对氨基苯甲酸(H2N![]() COOH)的合成路线(其他无机试剂任选)_____________。
COOH)的合成路线(其他无机试剂任选)_____________。
【答案】 O2N![]() COOH 硝基、羧基 取代
COOH 硝基、羧基 取代 ![]() CH3+HNO3(浓)
CH3+HNO3(浓)![]() O2N
O2N![]() CH3+H2O
CH3+H2O ![]() +CH3Cl
+CH3Cl![]()
![]() CH3+HCl 10
CH3+HCl 10 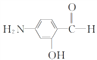
![]() CH3
CH3![]() O2N
O2N![]() CH3
CH3![]() O2N
O2N![]() COOH
COOH![]() H2N
H2N![]() COOH
COOH
【解析】根据O2N![]() COOCH2CH2N+H(C2H5)2·Cl-可知,F为对硝基苯甲酸,则E为对硝基甲苯,D为甲苯,与D的相对分子质量为92相符,试剂C为一氯甲烷。
COOCH2CH2N+H(C2H5)2·Cl-可知,F为对硝基苯甲酸,则E为对硝基甲苯,D为甲苯,与D的相对分子质量为92相符,试剂C为一氯甲烷。
根据![]() 结合反应② 的条件,结合B核磁共振氢谱只有1组峰可知, B为环氧乙烷。
结合反应② 的条件,结合B核磁共振氢谱只有1组峰可知, B为环氧乙烷。
(1) F为对硝基苯甲酸,结构简式为O2N![]() COOH,含有的官能团有硝基、羧基,故答案为:O2N
COOH,含有的官能团有硝基、羧基,故答案为:O2N![]() COOH;硝基、羧基;
COOH;硝基、羧基;
(2)反应④为甲苯发生的硝化反应,属于取代反应,化学方程式为![]() CH3+HNO3(浓)
CH3+HNO3(浓) ![]() O2N
O2N![]() CH
CH![]() CH3+HNO3(浓)
CH3+HNO3(浓) ![]() O2N
O2N![]() CH3+H2O;
CH3+H2O;
(3)反应③为苯与一氯甲烷的反应,反应的化学方程式为![]() +CH3Cl
+CH3Cl![]()
![]() CH3+HCl,故答案为:
CH3+HCl,故答案为:![]() +CH3Cl
+CH3Cl![]()
![]() CH3+HCl;
CH3+HCl;
(4)E为对硝基甲苯,既能发生银镜反应,含有醛基,又能遇FeCl3溶液显色,含有酚羟基,且不含酰胺键的芳香族同分异构体为苯环上含有羟基、氨基、醛基,共有10种同分异构体,如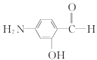 等,故答案为:10;
等,故答案为:10; ;
;
(5)由甲苯合成对氨基苯甲酸(H2N![]() COOH),可以首先在苯环上引入硝基,然后将甲基氧化为羧基,最后将硝基还原为氨基即可,合成路线为
COOH),可以首先在苯环上引入硝基,然后将甲基氧化为羧基,最后将硝基还原为氨基即可,合成路线为![]() CH3
CH3![]() O2N
O2N![]() CH3
CH3![]() O2N
O2N![]() COOH
COOH![]() H2N
H2N![]() COOH,故答案为:
COOH,故答案为:![]() CH3
CH3![]() O2N
O2N![]() CH3
CH3![]() O2N
O2N![]() COOH
COOH![]() H2N
H2N![]() COOH。
COOH。


科目:高中化学 来源: 题型:
【题目】(12分) 为测定NaOH、Na2C03混合物中Na2C03的质量分数,甲同学拟采用图(1)
所示装置来测定。乙同学拟采用图(2)所示装置来测定。
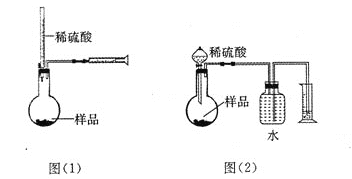
请回答下列问题:
(1)甲同学用图(1)装置来测定,在没有放样品前,检查该装置气密性的方法之一是从酸式滴定管向烧瓶中加入一定量的水,观察到 现象,证明此装量不漏气。实验时称得样品的质量为mg,酸式滴定管的起始读数为amL,终了读数为bmL,注射器测定排出的气体为c mL(已折算成标准状况),该样品中Na2C03的质量分数为(用含a、b、c、m的代数式表示)____ 。
(2)本实验选用稀H2S04而未选用稀盐酸的原因是 。
(3)乙同学观察了甲同学的实验后很受启发,并发现自己的图(2)原实验设计方案会造成误差.其原因之一可能是C02在水中溶解度较大,引起测量气体体积减小。
丙同学经思考后。建议乙同学将图(2)中某部分稍作改进,就可避免此种误差,写出你的改进方案 。
(4)丁同学提出将图(2)装置中量气装置去掉,只用反应装置和天平也能较准确地测出样品中Na2C03的质量分数,请你分析丁同学方案中,除了测定样品的质量,还需测定的另两个数据是 、 。
(5)还可以用其他实验方法测定试样中纯碱的质量分数,请简述一种与上述各方法不同的实验方法 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.淀粉和纤维素水解最终产物都是葡萄糖B.油脂水解可得到氨基酸和甘油
C.蛋白质水解的最终产物是多肽D.蔗糖在人体内水解产物只有葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中属于氧化还原反应,但水既不作氧化剂又不作还原剂的是( )
A.SO3+H2O=H2SO4
B.2Na2O2+2H2O=4NaOH+O2↑
C.2F2+2H2O=4HF+O2
D.2Na+2H2O=2NaOH+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某白色粉末由两种物质组成,为鉴别其成分进行如下实验:
①取少量样品加入足量水仍有部分固体未溶解;再加入足量稀盐酸,有气泡产生,固体全部溶解;
②取少量样品加入足量稀硫酸有气泡产生,振荡后仍有固体存在。
该白色粉末可能为( )
A. ![]() 、
、![]() B. AgCl、
B. AgCl、![]()
C. ![]() 、
、![]() D.
D. ![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石墨作电极电解100mLAgNO3溶液,通电一段时间后,两极均收集到2.24 L气体(标准状况),则原AgNO3溶液的物质的量浓度为( )
A. 3mol·L-1 B. 2mol·L-1 C. 1.5mol·L-1 D. 1mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某工业废水中含有大量FeSO4,较多的Cu2+, 以及部分污泥,通过下列流程可从该废水中回收FeSO4·7H2O晶体及金属Cu。

(1)步骤1的主要操作是___________,(填操作名称)需用到的玻璃仪器除烧杯外还有___________, ___________。
(2)步骤2中发生反应的离子方程式为______________________________
(3)步骤3中发生反应的化学方程式为______________________________
(4)步骤4中涉及的操作是:蒸发浓缩、________、过滤、洗涤、烘干。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制胆矾时,将粗制CuO粉末(含杂质FeO、Fe2O3)慢慢加入适量的稀H2SO4中完全溶解后,除去杂质离子后,再蒸发结晶可得纯净的胆矾晶体。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀.回答下列问题:
(1)为除去溶液中的Fe2+,可先加入______(填化学式)将Fe2+氧化为Fe3+,反应的离子方程式为__________,然后再加入适量的__________调整溶液的pH到______,使Fe3+转化为Fe(OH)3。
(2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=1×10-38,Cu(OH)2的溶度积Ksp=3×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 molL-1时就认为沉淀完全,设溶液中CuSO4的浓度为3molL-1,则Cu(OH)2开始沉淀时溶液的pH为______,Fe3+完全沉淀时溶液的pH为______,通过计算确定上述方案______ (填“可行”或“不可行”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com