
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得在不同时间(t)内产生气体体积(V)的数据如图所示,根据图示分析实验条件,下列说法中一定不正确的是( )
| 组别 | 对应曲线 | c(HCl)/mol·L-1 | 反应温度/℃ | 铁的状态 |
| 1 | a | 30 | 粉末状 | |
| 2 | b | 30 | 粉末状 | |
| 3 | c | 2.5 | 块状 | |
| 4 | d | 2.5 | 30 | 块状 |
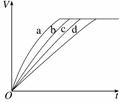
A.第4组实验的反应速率最慢
B.第1组实验中盐酸的浓度大于2.5 mol·L-1
C.第2组实验中盐酸的浓度等于2.5 mol·L-1
D.第3组实验的反应温度低于30 ℃
科目:高中化学 来源: 题型:
已知25 ℃时,FeS、CuS的溶度积常数(Ksp)分别为6.3×10-18、1.3×10-36。常温时下列有关说法正确的是( )
A.除去工业废水中的Cu2+可以选用FeS作沉淀剂
B.将足量CuSO4溶解在0.1 mol·L-1 H2S溶液中,Cu2+的最大浓度为1.3×10-35 mol·L-1
C.因为H2SO4是强酸,所以反应CuSO4+H2S===CuS↓+H2SO4不能发生
D.向H2S的饱和溶液中通入少量SO2气体,溶液的酸性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
氮的最高价氧化物为无色晶体,它由两种离子构成,已知其阴离子构型为平面三角形,则其阳离子的构型和阳离子中氮的杂化方式为( )
A.直线 sp杂化 B.V型 sp2杂化
C.三角锥形 sp3杂化 D.平面三角形 sp2 杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
聚合硫酸铁又称聚铁,化学式为[Fe2(OH)n(SO4)3-0.5n]m,广泛用于污水处理。实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4·7H2O),过程如下所示:
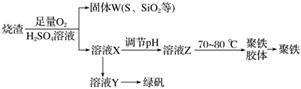
(1)验证固体W焙烧后产生的气体中含有SO2的方法是
________________________________________________________________________。
(2)制备绿矾时,向溶液X中加入过量__________,充分反应后,经__________操作得到溶液Y,再经浓缩、结晶等步骤得到绿矾。
(3)溶液Z的pH影响聚铁中铁的质量分数,用pH试纸测定溶液pH的操作方法为________________________________________________________________________。
若溶液Z的pH偏小,将导致聚铁中铁的质量分数________(填“偏大”或“偏小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应aA(g)+bB(g)cC(g)+dD(g),取a mol A和b mol B置于V L的容器中,1 min后,测得容器内A的浓度为x mol·L-1。这时B的浓度为______ mol·L-1,C的浓度为______ mol·L-1。这段时间内反应的平均速率若以物质A的浓度变化来表示,应为________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,10 mL 0.40 mol·L-1 H2O2溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表。
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)( )
A.0~6 min的平均反应速率:
v(H2O2)≈3.3×10-2 mol·L-1·min-1
B.6~10 min的平均反应速率:
v(H2O2)<3.3×10-2 mol·L-1·min-1
C.反应到6 min时,c(H2O2)=0.30 mol·L-1
D.反应到6 min时,H2O2分解了50%
查看答案和解析>>
科目:高中化学 来源: 题型:
某反应过程中能量变化如图所示,下列有关叙述正确的是( )
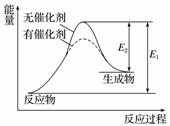
A.该反应为放热反应
B.催化剂改变了化学反应的热效应
C.催化剂不改变化学反应过程
D.催化剂改变了化学反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,充电时,总反应为Na2Sx === 2Na + xS(3<x<5),其反应原理如图所示,下列说法错误的是( )
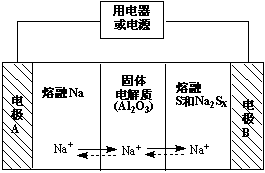
A.放电时,电极A为负极
B.该电池工作的适宜温度应控制10℃左右
C.放电时,内电路中Na+的移动方向为A到B
D.充电时,阳极的电极反应式为 Sx2- - 2e- === xS
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com