
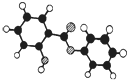
 萨罗(Salol)是一种消毒剂,为芳香族化合物,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等).则下列说法不正确的是( )
萨罗(Salol)是一种消毒剂,为芳香族化合物,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等).则下列说法不正确的是( )| A. | 萨罗的分子式为C13H10O3 | |
| B. | 1mol萨罗与浓溴水反应,需要消耗3mol Br2 | |
| C. | 1mol萨罗发生水解,需要消耗3mol NaOH | |
| D. | 萨罗经水解、分离、提纯可得到纯净的苯酚和水杨酸(邻羟基苯甲酸) |
分析 由球棍模型可知萨罗的结构简式 ,根据有机物结构简式可判断有机物元素种类和原子个数,可确定有机物分子式,有机物中含有酚羟基,可发生取代、氧化和颜色反应,含有酯基,可发生水解.
,根据有机物结构简式可判断有机物元素种类和原子个数,可确定有机物分子式,有机物中含有酚羟基,可发生取代、氧化和颜色反应,含有酯基,可发生水解.
解答 解:由球棍模型可知萨罗的结构简式 ,
,
A.由结构简式可知萨罗的分子式为C13H10O3,故A正确;
B.分子中酚羟基共有1个邻位和1个对位H原子可被取代,则1mol萨罗与浓溴水反应,需要消耗2mol Br2,故B错误;
C.有机物水解产物共含有2个酚羟基和1个羧基,则1mol萨罗发生水解,需要消耗3mol NaOH,故C正确;
D.由结构简式可知水解产物为苯酚和水杨酸,故D正确.
故选B.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于学生综合运用化学知识的能力的考查,注意根据有机物球棍模型判断有机物结构简式为解答该题的关键,并把握有机物官能团的性质,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | (A-N+3)mol | B. | $\frac{n}{A+106.5}$(A-N+51)mol | ||
| C. | $\frac{n}{A+35.5}$(A-N+51)mol | D. | $\frac{n}{A+106.5}$(A-N+47)mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
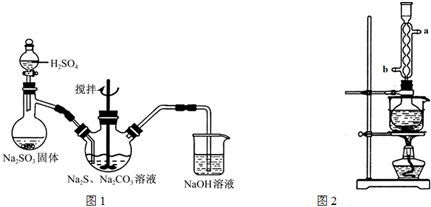
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
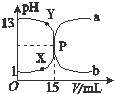 如图曲线a和b是盐酸与氧氧化钠溶液在常温下的相互滴定的滴定曲线,下列叙述中正确的是( )
如图曲线a和b是盐酸与氧氧化钠溶液在常温下的相互滴定的滴定曲线,下列叙述中正确的是( )| A. | 盐酸的物质的量浓度为1 mol•L-1 | |
| B. | P点时反应恰好完成,溶液呈中性,但它不是滴定终点 | |
| C. | X点时c(Cl-)>c(H+)>c(Na+)>c(OH-) | |
| D. | Y点时溶液呈碱性,溶液中c(H+)•c(OH-)>1×10-14 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③>①>④>② | B. | ①>②>③>④ | C. | ③>②>①>④ | D. | ①>④>③>② |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铊是易导电的银白色金属 | B. | 能生成+3价离子 | ||
| C. | 氢氧化铊是两性氢氧化物 | D. | Tl3+的氧化能力比Al3+弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol CO2中含有原子数NA | |
| B. | 1mol/L的硫酸钠溶液中,所含Na+数为2NA | |
| C. | 标准状况下,11.2 L水所含分子数为0.5 NA | |
| D. | 1 mol Fe和足量盐酸完全反应失去的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com