下列说法正确的是( )
A.一定温度、压强下,气体体积由其分子的大小决定
B.等物质的量的氧气和臭氧(O3)的体积一定相同
C.同温同压下,体积相同的N2和CO,分子数一定相同
D.同温同压下,等质量的CH4和SO2分子数比为1:4
【答案】
分析:A.气体粒子之间的距离远远大于粒子本身的直径,当粒子数一定,气体的体积主要决定于气体粒子之间的距离;
B.根据V=nVm确定其体积相对大小;
C.同温同压下,气体摩尔体积相同,等体积的气体物质的量相同,根据N=nN
A确定分子数;
D.根据N=nN
A=

确定分子数.
解答:解:A.气体粒子间距离较大,远大于粒子的直径,所以粒子大小可以忽略不计,决定气体体积的因素主要为构成物质的粒子数和粒子间的距离,一定质量的气体,气体的分子数目一定,故一定温度下,影响一定质量气体体积大小的决定因素是气体分子间的平均距离,故A错误;
B.气体摩尔体积与温度和压强有关,温度和压强未知导致气体摩尔体积未知,所以无法判断其体积大小,故B错误;
C.同温同压下,气体摩尔体积相同,等体积的气体物质的量相同,则由N=nN
A知,所含分子数相等,故C正确;
D.由N=nN
A=
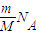
知,等质量的CH
4和SO
2,含有的分子数与摩尔质量成反比,甲烷的摩尔质量是16g/mol,二氧化硫的是64g/mol,所以等质量的CH
4和SO
2分子数比为4:1,故D错误;
故选C.
点评:本题考查了阿伏伽德罗定律及推论,注意有关气体体积的计算要考虑温度和压强,但计算分子数或原子数、质量等不用考虑气体的温度和压强,为易错点.

 确定分子数.
确定分子数.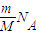 知,等质量的CH4和SO2,含有的分子数与摩尔质量成反比,甲烷的摩尔质量是16g/mol,二氧化硫的是64g/mol,所以等质量的CH4和SO2分子数比为4:1,故D错误;
知,等质量的CH4和SO2,含有的分子数与摩尔质量成反比,甲烷的摩尔质量是16g/mol,二氧化硫的是64g/mol,所以等质量的CH4和SO2分子数比为4:1,故D错误;


 Sn(s,白)△H3=+2.1kJ?mol-1,
Sn(s,白)△H3=+2.1kJ?mol-1,