
【题目】电化学降解NO3﹣的原理如图所示.
(1)电源A极为_____(填“正极”或“负极”),阴极反应式为_____。
(2)若电解过程中转移了1mol电子,则膜左侧电解液的质量减少量为_____g。

【答案】正极 2NO3﹣+10e﹣+12H+=6H2O+N2↑ 9
【解析】
(1)根据图象知,硝酸根离子得电子发生氧化反应,则Ag-Pt作阴极,Pt电极为阳极,A为正极,B为负极,以此解答该题;
(2)由图示知在Ag-Pt电极上NO3-发生还原反应,因此Ag-Pt电极为阴极,则B为负极,A为电源正极,转移1mol电子时,计算阳极上消耗的水的量以及进入阴极室的阳离子的量,进而计算质量的变化。
(1)由图示知在Ag-Pt电极上NO3-发生还原反应,因此Ag-Pt电极为阴极,则B为负极,A为电源正极。在阴极反应是NO3-得电子发生还原反应生成N2,利用电荷守恒与原子守恒知有H2O参与反应且有水生成,所以阴极上发生的电极反应式为:2NO3-+12H++10e-=N2+6H2O;
(2)由图示知在Ag-Pt电极上NO3-发生还原反应,因此Ag-Pt电极为阴极,则B为负极,A为电源正极,转移1mol电子时,阳极(阳极反应为H2O失电子氧化为O2和H+)消耗0.5mol水,产生1mol H+进入阴极室,阳极室质量减少9g。


 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:
【题目】下图是由常见元素组成的一些单质及其化合物之间的转化关系图。各方框表示有关的一种反应物或生成物(部分物质已经略去)。其中A、B、D在常温下均为无色无味的气体,C是能使湿润的红色石蕊试纸变蓝的气体,M是最常见的无色液体。

(1)写出C→E的化学方程式: 。
(2)实验室常用加热两种固体混合物的方法制备物质C,其化学方程式为: ,干燥C常用 (填写试剂名称)。
(3)E物质遇到D物质时,会观察到 现象,若用排水法收集F,则最终集气瓶中收集到的气体为 (填写物质的化学式)。
(4)写出A→D的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某物质溶于盐酸后,再向溶液中滴加硫氰化钾溶液,结果溶液颜色无变化,然后加入新制氯水,溶液呈红色,则这种物质是( )
A.氯化铁B.氯化亚铁C.氢氧化铁D.四氧化三铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学”是当今社会提出的一个新概念,在“绿色化学工艺”中理想状态是反应物的原子全部转化为目标产物,即原子利用率为100%。下列过程符合“绿色化学”理念的是
A. 实验室制O2:2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
B. 2C2H5OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
C. 2M+N=2P+2Q,2P+M=Q(M、N为原料,Q为期望产品)
D. 用铁屑、CuO、稀硫酸为原料制铜:CuO+H2SO4=CuSO4+H2O、Fe+CuSO4=FeSO4+Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4molA气体和2molB气体在2L的密闭容器中混合,并在一定条件下发生如下反应:2A(g)+B(g)![]() xC(g),若经2s后测得A的物质的量为2.8mol,C的物质的量浓度为0.6mol/L。以下说法中正确的是
xC(g),若经2s后测得A的物质的量为2.8mol,C的物质的量浓度为0.6mol/L。以下说法中正确的是
A. 2s内物质A的平均反应速率为0.6mol-1·l-1·s-1 B. 2s时物质B的转化率为70%
C. 2s内物质B的平均反应速率为0.6mol-1·l-1·s-1 D. x=2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用下图表示。

(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是_________(填图中数字序号)。
(2)下列关于海洋氮循环的说法正确的是__________(填字母序号)。
a. 海洋中存在游离态的氮
b. 海洋中的氮循环起始于氮的氧化
c. 海洋中的反硝化作用一定有氧气的参与
d. 向海洋排放含NO3-的废水会影响海洋中NH4+的含量
(3)有氧时,在硝化细菌作用下,NH4+可实现过程④的转化,将过程④的离子方程式补充完整:_____NH4+ + 5 O2==2 NO2- + ___ H+ + ______+ _______
(4)有人研究了温度对海洋硝化细菌去除氨氮效果的影响,下表为对10 L人工海水样本的监测数据:
温度/℃ | 样本氨氮含量/mg[ | 处理24 h[] | 处理48 h |
氨氮含量/mg | 氨氮含量/mg | ||
20 | 1008 | 838 | 788 |
25 | 1008 | 757 | 468 |
30 | 1008 | 798 | 600 |
40 | 1008 | 977 | 910 |
硝化细菌去除氨氮的最佳反应温度是______,在最佳反应温度时,48 h内去除氨氮反应的平均速率是______________mg·L-1·h-1。
(5)为了避免含氮废水对海洋氮循环系统的影响,需经处理后排放。图是电解产物氧化工业废水中氨氮(NH4+)的示意图。

①阳极的电极反应式:____________________;
②写出电解产物氧化去除氨氮的离子方程式:____________;
③若生成H2和N2的物质的量之比为3:1,则处理后废水的c(H+)将________(填“增大”、“不变”或“减小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E五种元素为周期表前20号元素且原子序数依次增大,其中只有A、D为非金属元素。A的气态氢化物溶于水得到的溶液能使酚酞溶液变红。B、C、D的最高价氧化物对应水化物相互之间能够两两反应,且D原子最外层电子数是C原子最外层电子数的2倍。B、E元素同主族。
(1)E在元素周期表中的位置:____________,写出E的最高价氧化物对应水化物与C的单质反应的化学方程式:___________________________________。
(2)A的气态氢化物溶于水后的电离方程式为________________________________。
(3)B单质在空气中燃烧后的产物的电子式为____________,产物中存在的化学键类型有_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别按下图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中A为电流表。请回答下列问题:
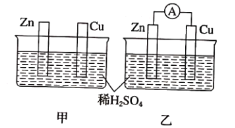
(1)以下叙述中,正确的是_______(填字母).
A 甲中锌片是负极,乙中铜片是正极 B 两烧杯中铜片表面均有气泡产生
C 两烧杯中溶液pH均增大 D 产生气泡的速度甲中比乙中慢
E 乙的外电路中电流方向Zn→Cu F 乙溶液中SO42-向铜片方向移动
(2)变化过程中能量转化的主要形式:甲为_________;乙为________。
(3)在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是____。
(4)在乙实验中,如果把硫酸换成硫酸铜溶液,请写出铜电极的电极反应方程式:__________,当电路中转移0.25mo1电子时,消耗负极材料的质量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(6分)某课外活动小组同学用如图装置进行实验,试回答下列问题。

(1)若开始时开关K与b连接,则B极的电极反应式为 。
总反应的离子方程式为 。
有关上述实验,下列说法正确的是(填序号) 。
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电解质相同的状态(质量和浓度均相同)
④若标准状况下B极产生2.24 L气体,则电路中转移0.2 mol电子
(2)若开始时开关K与a连接,则B极的电极反应式为
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com