
| A. | 2gH2中的原子数目为NA | |
| B. | 64gSO2中的原子数目为3NA | |
| C. | 1mol/LNaOH溶液中的Na+的数目为NA | |
| D. | 常温常下,11.2LCl2中的分子数目为0.5NA |
分析 A.依据n=$\frac{m}{M}$结合氢气为双原子分子解答;
B.依据n=$\frac{m}{M}$结合1个二氧化硫分子含有3个原子解答;
C.溶液体积未知;
D.常温下,Vm>22.4L/mol.
解答 解:A.2gH2中的原子数目为$\frac{2g}{2g/mol}$×2×NA=2NA,故A错误;
B.64gSO2中的原子数目为$\frac{64g}{64g/mol}$×3×NA=3NA,故B正确;
C.依据n=CV可知,溶液体积未知,无法计算钠离子数目,故C错误;
D.常温下,Vm>22.4L/mol,常温常下,11.2LCl2中的分子数目小于0.5NA,故D错误;
故选:B.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大.


 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X的简单气态氢化物的热稳定性比Y的强 | |
| B. | W的氧化物的水化物的酸性一定比X的强 | |
| C. | 半径r(W)>r(Z)>r(Y)>r(X) | |
| D. | Z与Y形成的两种常见化合物中,阴、阳离子个数比均为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 |
| A | 将浸透了石蜡油的石棉放在大试管底部.试管中加人碎 瓷片,给碎瓷片加强热,产生的气体持续通入溴的四氯化碳溶液 | 红棕色逐渐变浅,最终褪去 |
| B | 将乙烯在空气中点燃 | 火焰呈蓝色并伴有黑烟 |
| C | 向盛有苯的试管中加入几滴酸性KMnO溶液,充分振荡 | 液体分层,溶液紫色褪去 |
| D | 将蔗糖溶液与稀硫酸混合水浴加热,取反应后的溶液少量.加人几滴新制的Cu(OH)2悬浊液加热 | 出现砖红色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室中,可用金属钠检验乙醇中是否含有水 | |
| B. | 甲烷是天然气的主要成分,能发生取代反应,但不能发生氧化反应 | |
| C. | 只用水无法鉴别苯、乙酸和四氯化碳 | |
| D. | 植物油不能用于萃取溴水中的溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将NaH溶于水,得到的水溶液能导电说明NaH是离子化合物 | |
| B. | Fe(OH)3胶体和Fe(OH)3沉淀的化学性质不相同 | |
| C. | 乙醇分子中含羟基,可与金属钠反应生成氢气 | |
| D. | MnO2具有较强氧化性,可作为H2 O2分解反应的氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
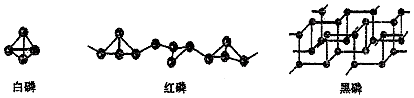
| A. | 属于同位素 | B. | 属于同分异构体 | ||
| C. | 都属于多原子分子 | D. | 黑磷在空气中不易燃烧 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com