
����Ŀ����һ������þ��ͭ��ɵĻ������뵽ϡ�����У�������ȫ�ܽ�(���跴Ӧ�л�ԭ����ֻ��NO)����Ӧ�����Һ�м���3 mol��L1NaOH��Һ��������ȫ��������ɳ�����������ԭ�Ͻ����������5.1 g��������������ȷ����
A. ������ȫ���ܽ�ʱ���μӷ�Ӧ����������ʵ���һ����0.4mol
B. �μӷ�Ӧ�Ľ�����������3.6g<m<9.6g
C. �����ɵij������ﵽ���ʱ������NaOH��Һ�����һ��ΪV=100mL
D. ������ȫ���ܽ�ʱ�ռ���NO���������ڱ�״����Ϊ2.24L
���𰸡�C
��������
��һ������þ��ͭ��ɵĻ������뵽ϡHNO3�У�������ȫ�ܽ⣨���跴Ӧ�л�ԭ����ֻ��NO����������Ӧ��3Mg+8HNO3 ��ϡ��=3Mg��NO3��2+2NO��+4H2O��3Cu+8HNO3 ��ϡ��=3Cu��NO3��2+2NO��+4H2O����Ӧ�����Һ�м��������3mol/LNaOH��Һ��������ȫ��������Ӧ��Mg��NO3��2+2NaOH=Mg��OH��2��+2NaNO3��Cu��NO3��2+2NaOH=Cu��OH��2��+2NaNO3������Ϊ������þ��������ͭ�����ɳ�����������ԭ�Ͻ����������5.1g����������þ��������ͭ����������������Ϊ5.1g�������������ʵ���Ϊ![]() =0.3mol�����ݵ���ת���غ㣬��þ��ͭ���ܵ����ʵ���Ϊ0.15mol��A�����ݷ���ʽ��֪�μӷ�Ӧ��n��Ӧ��HNO3��=
=0.3mol�����ݵ���ת���غ㣬��þ��ͭ���ܵ����ʵ���Ϊ0.15mol��A�����ݷ���ʽ��֪�μӷ�Ӧ��n��Ӧ��HNO3��=![]() n��������=0.15mol��
n��������=0.15mol��![]() =0.4mol����A��ȷ��B��þ��ͭ���ܵ����ʵ���Ϊ0.15mol���ٶ�ȫΪþ������Ϊ0.15mol��24g/mol=3.6g����ȫΪͭ������Ϊ0.15mol��64g/mol=9.6g�����Բμӷ�Ӧ�Ľ�������������m��Ϊ3.6g��m��9.6g����B��ȷ��C����������ʣ�࣬��μӷ�Ӧ�������Ƶ����ʵ���Ϊ0.3mol����Ҫ����������Һ���Ϊ��
=0.4mol����A��ȷ��B��þ��ͭ���ܵ����ʵ���Ϊ0.15mol���ٶ�ȫΪþ������Ϊ0.15mol��24g/mol=3.6g����ȫΪͭ������Ϊ0.15mol��64g/mol=9.6g�����Բμӷ�Ӧ�Ľ�������������m��Ϊ3.6g��m��9.6g����B��ȷ��C����������ʣ�࣬��μӷ�Ӧ�������Ƶ����ʵ���Ϊ0.3mol����Ҫ����������Һ���Ϊ��![]() =0.1L=100mL����������ʣ�࣬���ĵ�����������Һ�������100mL������V��100mL����C����D�����ݵ���ת���غ��֪���ɵ�NO���ʵ���Ϊ
=0.1L=100mL����������ʣ�࣬���ĵ�����������Һ�������100mL������V��100mL����C����D�����ݵ���ת���غ��֪���ɵ�NO���ʵ���Ϊ![]() =0.1mol����״���£�����NO�����Ϊ0.1mol��22.4L/mol=2.24L����D��ȷ����ѡC��
=0.1mol����״���£�����NO�����Ϊ0.1mol��22.4L/mol=2.24L����D��ȷ����ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾΪ��˫ɫ˫��Ȫ��ʵ��װ�ã�ͼ����ƿ�ڷֱ�����������Ȼ��⣬�ձ���ʢװ����ʯ����Һ������ˮ������˵���������

A. ��ʵ�����У�����Ũ��ˮ����ʯ���Ʊ���������Ũ�����Ũ�����Ʊ��Ȼ���
B. ��ʵ�������Ʊ�����İ������Ȼ���ʱ����ѡ����ͬ�ĸ����
C. ʵ����ͬʱ��ֹˮ��a��c��d�����ɷֱ��γ���ɫ�ͺ�ɫ��Ȫ
D. ��Ȫ��������ƿ����Һ��Ϻ����ɫ�����ɿɵ��Ȼ�粒���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У�����ˮ����Ũ����������������ռ��������������KMnO4��Һ��������һ�������¿�������鷢����ѧ��Ӧ���� ( )
A. �٢ڢۢ� B. �ܢݢ� C. �ۢ� D. �ڢۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA��ʾ�����ӵ�������ֵ������������ȷ����
A. 18 g D2O�����ĵ�����Ϊ10NA
B. 1 mol H2O2�к��м��Լ�����ĿΪ3NA
C. ��״���£�22.4 L���Ȼ�̼����������ΪNA
D. 32g O2��O3�Ļ�����к��е���ԭ����Ϊ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A.�ƼغϽ�ͨ��״���³�Һ̬������ԭ�ӷ�Ӧ�ѵĵ��ȼ�
B.�ƵĻ�ѧ���ʻ��ã��������ƿɱ������л��ܼ����Ȼ�̼��
C.���ڿ����л�����������ȼ����������ȼ�ո�Ϊ����
D.����������ͭ��Һ�����û���Ӧ���ɵ���ͭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����þ����һ�ֹ�ҵ���ϣ���Ҫ�ɷ���MgO��ռ40%������������������CaO��MnO��Fe2O3��FeO��Al2O3��SiO2�����ʣ��Դ�Ϊԭ����ȡ������þ��������ӡȾ����ֽ��ҽҩ�ȹ�ҵ������þ������ȡMgSO47H2O�Ĺ����������£�
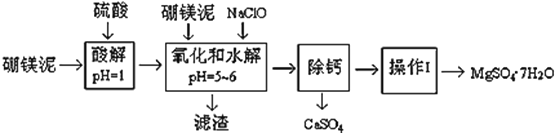
��1��ʵ������Ҫ1 mol/L������800 mL������ 98% ��Ũ���ᣨ��= 1.84 g/mL�������ƣ���ȡŨ������Ҫʹ����Ͳ�Ĺ��Ϊ__________����дѡ����ĸ��
A��10 mL B��20 mL C��50 mL D��100 mL
��2�������NaClO����Mn2+ ��Ӧ��Mn2+ + ClO + H2O = MnO2��+ 2H+ + Cl ���ڸò����л���һ������Ҳ�ᱻNaClO�������÷�Ӧ�����ӷ���ʽΪ___________________��
��3����������Ҫ�ɷֳ�����Fe(OH)3��Al(OH)3�⣬������__________��___________��
��4���ڡ����ơ�ǰ���������Һ��Fe3+ �Ƿ������������鷽��___________________����д������������ͽ��ۣ�
��5����֪MgSO4��CaSO4 ���ܽ�ȣ���λΪ g/100 g ˮ�����±���
�¶ȣ��棩 | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
�����ơ��ǽ�MgSO4��CaSO4�����Һ�е�CaSO4��ȥ�������ϱ����ݣ���Ҫ˵����������______�����������ǽ���Һ��������Ũ������ȴ�ᾧ��______����õ���MgSO47H2O
��6��ʵ�����ṩ����þ�100 g���õ� MgSO47H2OΪ172.2 g ����MgSO47H2O �IJ���Ϊ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˱������¸ֹܲ��ܸ�ʴ����ʹ���루 ��
A.ֱ����Դ��������B.ͭ������
C.Ǧ������D.ֱ����Դ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ����д�����۾���������( )
ѡ�� | ���ӷ���ʽ | ���� |
A | ��2 mol Cl2ͨ�뺬1 mol FeI2����Һ�У� 2Fe2����2I����2Cl2===2Fe3����4Cl����I2 | ��ȷ��Cl2�������ɽ�Fe2����I�������� |
B | Ba(HCO3)2��Һ��������NaOH��Һ��Ӧ�� Ba2����HCO3-��OH��===BaCO3����H2O | ��ȷ����ʽ����Ӧ�������κ�ˮ |
C | ����SO2ͨ��NaClO��Һ�У� SO2��H2O��ClO��===HClO��HSO3- | ��ȷ��˵�����ԣ�H2SO3ǿ��HClO |
D | 1 mol/L��NaAlO2��Һ��2.5 mol/L��HCl��Һ�������ϣ� 2AlO2-��5H��===Al3����Al(OH)3����H2O | ��ȷ����һ����Ӧ�͵ڶ�����Ӧ���ĵ�H�������ʵ���֮��Ϊ2��3 |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ�������ѧ���ļ������γ�(���)1 mol��ѧ��ʱ�ͷ�(������)����������֪����P4O6�ķ��ӽṹ����ͼ��ʾ�����ṩ���»�ѧ���ļ���(kJ��mol��1)P��P��198 P��O��360 O��O��498����ӦP4(����)��3O2===P4O6�������仯Ϊ�� ��

A���ͷ�1638 kJ������
B������1638 kJ������
C���ͷ�126 kJ������
D������126 kJ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com