

分析 (1)Ⅰ.Mg可以与CO2、N2发生化学反应,Mg与氢气不能发生反应;
Ⅱ.(不纯的氢气燃烧会发生爆炸;Mg与SiO2反应的条件是加热,切断电源后,反应的条件由反应放热维持;
(2)①浓硫酸和亚硫酸钠反应生成二氧化硫气体,二氧化硫与Mg反应,生成淡黄色固体S,臭鸡蛋气味的气体为硫化氢,因此二氧化硫与Mg反应产物为MgS.根据元素守恒可知,另外一种产物为氧化镁;
②Mg能与空气中的氧气、氮气及二氧化碳反应,C中发生反应前需要除去装置内的空气;
③打开K,将空气充入反应反应体系,可平衡容器内外压强,防止倒吸;
④玻璃的主要成分含有二氧化硅,Mg也能和二氧化硅反应生成氧化镁和硅,结合原子守恒,写出此反应的化学方程式.
解答 解:(1)Ⅰ.Mg可以与CO2、N2发生化学反应,3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2、2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,Mg与氢气不能发生反应,因此可用氢气作为保护气,故选③;
Ⅱ.装置中有空气,若不用氢气排空装置中的空气,氢气和空气的混合气体燃烧会发生爆炸;Mg与SiO2反应的条件是加热,切断电源后,反应的条件由反应放热维持,
故答案为:防止加热条件下H2与空气混合爆炸;Mg与SiO2的反应是放热反应;
(2)①浓硫酸和亚硫酸钠反应生成二氧化硫气体,二氧化硫与Mg反应,生成淡黄色固体S,臭鸡蛋气味的气体为硫化氢,因此二氧化硫与Mg反应产物为MgS.根据元素守恒可知,另外一种产物为MgO,
故答案为:MgO、S、MgS;
②在加热C装置前,需要使A中反应进行,这样可以利用SO2除去装置内的空气,防止镁与空气中的氧气、氮气及二氧化碳反应,故答案为:赶尽空气,防止空气氧化镁粉;
③停止实验后,温度降低导致体系内部压强减小,容易发生倒吸,打开K,将空气充入反应反应体系,可平衡容器内外压强,防止倒吸,
故答案为:防止C管降温时因气体压强减小,而引起D中溶液倒流;
④Mg与玻璃中的二氧化硅在高温下反应的化学方程式为2Mg+SiO2$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+Si,故答案为:2Mg+SiO2$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+Si.
点评 本题考查了物质实验室制备原理和装置选择,实验步骤的设计分析判断,物质性质的应用是解题关键,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 溶液是电中性的,胶体是带电的 | |
| B. | CO2的水溶液能导电,所以CO2为电解质 | |
| C. | 可使用丁达尔效应来区分FeCl3溶液和Fe(OH)3胶体 | |
| D. | 1 mol 任何物质均含有约6.02×1023个原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
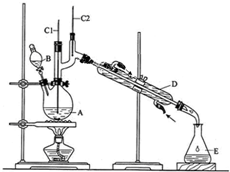
| 沸点/℃ | 密度/g•cm-3 | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:| 相对分子质量 | 密度/(g•cm3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
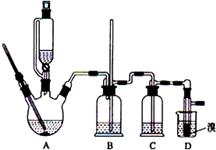 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | 液溴 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 | 红色发烟液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 | 3.12 |
| 沸点/℃ | 78.5 | 132 | 34.6 | 58.8 |
| 熔点/℃ | -l30 | 9 | -1l6 | -7.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ①③⑤④② | C. | ①⑤④③② | D. | ①②⑤③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用澄清石灰水鉴别Na2CO3和NaHCO3溶液 | |
| B. | 用焰色反应鉴别NaCl和KCl | |
| C. | 用丁达尔效应鉴别硫酸钠溶液和硅酸胶体 | |
| D. | 用排水集气法收集NO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com