
【题目】在粗盐提纯的实验中,蒸发时正确的操作是( )
A.把浑浊的液体倒入蒸发皿内加热
B.开始析出晶体后用玻璃棒搅拌
C.待水分完全蒸干后停止加热
D.蒸发皿中出现大量固体时即停止加热
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列有关氨的性质的叙述中,正确的是
A.氨水是一种强碱B.氨气和酸都能在空气中相遇产生白色烟雾
C.液氨常用来做致冷剂D.氨的分子结构呈正四面体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知质量分数为25%的氨水密度是0.91g·cm-3,质量分数为5%的氨水密度是0.98 g·cm-3,若将上述两溶液等体积混合,所得氨水的质量分数是
A. 等于15% B. 小于15% C. 大于15% D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有浓度均为0.1molL﹣1的盐酸、硫酸和醋酸三种溶液,试分析:
(1)若溶液的C(H+)分别为a、b、c,则它们的大小关系是(用“>”“<”“=”表示),
(2)分别用三种酸中和等物质的量的氢氧化钠溶液,所需溶液的体积分别是a、b、c,则它们的大小关系是(用“>”“<”“=”表示).
(3)等体积的三种酸分别与足量的锌粒反应,在相同条件下若产生气体的体积分别为a、b、c,则它们的关系是 .
(4)可逆反应2Cl2(g)+2H2O(g)4HCl(g)+O2(g)△H>0,在一定条件下达到平衡后,分别采取下列措施(填“增大”、“减小”或“不变”):
①降低温度,Cl2的转化率;
②保持容器体积不变,加入He,则HCl的物质的量;
③保持容器压强不变,加入He,则O2的体积分数 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是( )
A.Fe ![]() FeCl2
FeCl2 ![]() Fe(OH)2
Fe(OH)2
B.S ![]() SO3
SO3 ![]() H2SO4
H2SO4
C.CaCO3 ![]() CaO
CaO ![]() CaSiO3
CaSiO3
D.NH3 ![]() NO
NO ![]() HNO3
HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物A,含有Al2(SO4)3、Al2O3和Fe2O3,在一定条件下可实现下图所示的变化。请回答下列问题。
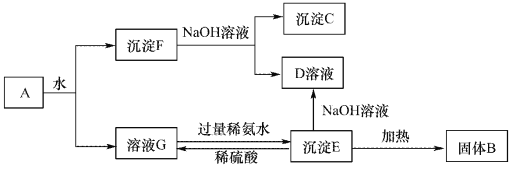
(1)沉淀F与NaOH溶液反应的离了方程式为_______________。
(2)沉淀C与稀硫酸反应的离子方程式为_______________。
(3)溶液G与过量稀氨水反应的化学方程式为_______________。
【答案】 Al2O3 + 2 OH-=AlO2-+H2O Fe2O3 + 6H+ =2 Fe3++3H2O Al2(SO4)3 + 6NH3·H2O = 2Al(OH)3↓ + 3(NH4)2SO4
【解析】根据流程可知:A溶于水得沉淀和溶液,溶液G是硫酸铝溶液,沉淀F是氧化铝和氧化铁;
将沉淀F溶于过量NaOH溶液中,Al2O3能和氢氧化钠反应,Fe2O3和氢氧化钠不反应,所以沉淀C是Fe2O3,溶液D是NaAlO2;溶液G中加入过量的氨水得到沉淀E,则E为Al(OH)3,Al(OH)3与NaOH溶液反应得到NaAlO2,将Al(OH)3加热得到沉淀B,B是Al2O3,硫酸铝和氨水反应生成Al(OH)3和硫酸铵,(1)沉淀F与NaOH溶液反应的离子方程式为:Al2O3 + 2 OH-=AlO2-+H2O;(2)沉淀C为Fe2O3,Fe2O3与稀硫酸反应的离子方程式为:Fe2O3 + 6H+ =2 Fe3++3H2O;(3)溶液G与过量稀氨水反应的化学方程式为:Al2(SO4)3 + 6NH3·H2O = 2Al(OH)3↓ + 3(NH4)2SO4。
点睛:本题考查了常见物质的分离与提纯方法综合应用,完成此类题目,可以依据题干提供的信息,结合框图,找准解题的突破口,直接得出物质,然后顺推或逆推或由两边向中间推得出其他物质,A溶于水得沉淀F和溶液G,硫酸铝易溶于水,氧化铝、氧化铁不易溶于水,所以得到的溶液G为硫酸铝溶液,沉淀F为氧化铝和氧化铁;将沉淀F溶于过量氢氧化钠溶液中,氧化铝能与氢氧化钠反应,氧化铁与氢氧化钠不反应,所以沉淀C是Fe2O3,溶液D是NaAlO2溶液,溶液G中加入过量的氨水得到沉淀E为Al(OH)3,Al(OH)3与NaOH溶液反应得到NaAlO2,将Al(OH)3加热得到沉淀B,B是氧化铝,硫酸铝和氨水反应生成氢氧化铝和硫酸铵,据此进行解答。
【题型】综合题
【结束】
27
【题目】图中是实验室制备SO2并验证SO2某些性质的装置图。试回答:
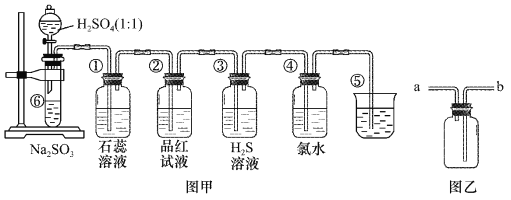
(1)如果用浓硫酸和铜来制取SO2,发生装置还需选用的仪器是________,化学方程式为_________ 。
(2)⑤的作用是________,反应的离子方程式为________ 。
(3)选用图乙收集SO2气体,气体从________ 口 进。
(4)填表格
装置 | 实验现象 | 体现SO2的性质 |
① | ____________ | ____________ |
② | ___________ | ____________ |
③ | ____________ | ____________ |
④ | ____________ | ____________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g)→C(g)△H,分两步进行:①A(g)+B(g)→X(g)△H1 , ②X(g)→C(g)△H2 , 反应过程中能量变化如图所示,E1表示A(g)+B(g)→X(g)的活化能,下列说法正确的是( ) 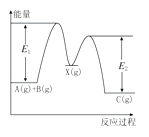
A.△H=E1﹣E2
B.E1是反应①的活化能
C.X是反应A(g)+B(g)→C(g)的催化剂
D.△H2>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓盐酸瓶打开,瓶口往往会形成白色的酸雾,这是因为
①浓盐酸有挥发性,挥发出HCl气体;②天气较潮湿,空气中水气较多;③浓盐酸因溶有少量Fe3+,而显黄色;④HCl气体极易溶于水
A.①②③B.①②④C.①④D.①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学欲配制100mL0.10mol·L-1的CuSO4溶液。以下操作1~5是其配制的过程及示意图:

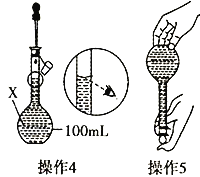
(1)操作1:准确称取__________g的胆矾晶体(化学式为CuSO45H2O)并用适量蒸馏水溶解。
(2)操作2:将所得溶液转移到__________(填仪器X的名称)中,用蒸馏水冲洗烧杯和玻璃棒2~3次,将洗涤液也转移到X中。
(3)操作3:继续向X中加蒸馏水至液面离X的刻度线1~2cm处。
(4)若其余操作步骤均正确,根据操作4所配的溶液浓度_________(填“偏大”、“偏小”、“不影响”或“无法判断”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com