
科目:高中化学 来源:不详 题型:单选题
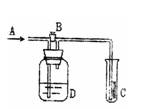
| A.用“化冰盐”融雪属于化学变化 |
| B.估计MgCl2也可用作“化冰盐” |
| C.使用“化冰盐”可使水分子结构发生变化 |
| D.大量使用这些“化冰盐”不会造成环境污染 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
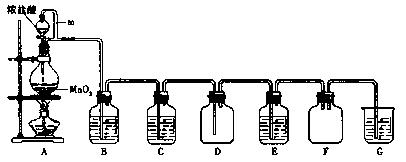
 。
。 b.稀盐酸滴人MnO2中,然后加入NaCl固体,加热
b.稀盐酸滴人MnO2中,然后加入NaCl固体,加热查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氧化物 | B.酸 | C.碱 | D.盐 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.得0.2 mol NaCl和0.08 NaHCO3 |
B.剩0.04 mol Na2CO3 ,得0.2 mol NaCl ,得0.2 mol NaCl |
| C.剩0.06 mol HCl,得0.14 mol NaCl和0.14 mol NaHCO3 |
| D.得0.06 mol NaCl和0.08 NaHCO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.转移0.5 mol电子 | B.生成0.5 mol Cl2 |
| C.参加反应的HC1为1.6 mol | D.Cl2是还原产物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.单质的颜色逐渐加深 | B.气态氢化物的稳定性逐渐增强 |
| C.与氢气反应越来越容易 | D.单质的熔、沸点逐渐降低 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com