
| 甲 | 乙 | | ||||||||||||||||||||
| 丙 | 丁 | 戊
练习册系列答案
相关习题
科目:高中化学 来源:不详 题型:填空题 (7分)已知某粒子的结构示意图为 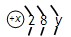 试回答: (1)当x-y=10时,该粒子为 (填“原子”、“阳离子”或“阴离子”) (2)写出y =3与y =7的元素最高价氧化物对应水化物间发生反应的离子方程式: 。 (3)当y=8时,粒子可能为 。 查看答案和解析>> 科目:高中化学 来源:不详 题型:填空题 已知D、E、F均是短周期元素形成的单质, E的氧化物对应的水化物为中强碱,F为黑色固体, A、D为无色气体,B、C的焰色反应呈黄色。它们之间的变化关系如右图所示(个别生成物略去),回答以下问题: 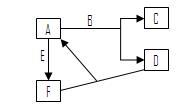 (1)写出A与E反应的化学方程式: 。 (2)写出与E同周期的最活泼非金属单质的实验室制法的化学方程式: 。 (3)写出C的溶液与少量盐酸反应的离子方程式: 。 查看答案和解析>> 科目:高中化学 来源:不详 题型:填空题 阅读资料,获取信息,回答问题。 (A) A、 B、C、D为四种元素,A原子的1S轨道为半充满;在元素周期表中,B的电负性最大;C的原子序数为24;D2+的电子排布式和Ar相同。 (B)两元素电负性差值大于1. 7,原子间一般形成离子键;小于1. 7,原子间一般形成共价键。 (C)下列是周期表中部分元素的电负性x和第一电离能I1 (KJ·mol-1): 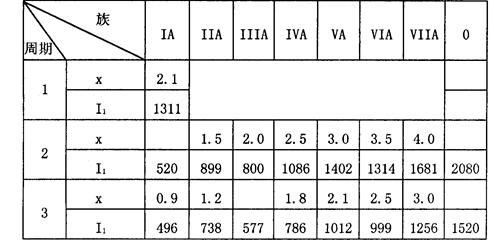 (1).A原子的轨道表示式为 ,B原子的价电子排布式为 ,C原子的电 子排布式为 ,D在周期表中的位置为________周期________族。 (2).电负性最小的元素位于 族,第一电离能最大的元素是(填元素符号) ; 锂元素的电负性取值范围为 <x(Li)< ;A12S3属 化合物 (3)标出化合物OF2、 LiAlH4中各元素的化合价(写在元素符号上)。 查看答案和解析>> 科目:高中化学 来源:不详 题型:单选题 短周期元素X、Y、Z在元素周期表中的位置如下图所示。下列说法正确的是 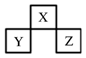
查看答案和解析>> 科目:高中化学 来源:不详 题型:单选题 某主族元素的原子最外层电子排布是5s1,下列描述中正确的是
查看答案和解析>> 科目:高中化学 来源:不详 题型:单选题 下列关于原子半径的周期性变化描述不严谨的是
查看答案和解析>> 科目:高中化学 来源:不详 题型:单选题 关于碱金属元素的表述正确的是
查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |