
����Ŀ��ij��Һ�п��ܺ���H+��Na+��NH4+��Mg2+��Fe3+��Al3+��SO42�������ӣ��������Һ�м���ijŨ�ȵ�NaOH��Һʱ���������ɳ��������ʵ�����NaOH��Һ������仯��ͼ��ʾ�������йضԸ���Һ���жϲ���ȷ���ǣ�������

A. ����Һ�п϶����е�������H+��NH4+��Al3+��SO42��
B. �϶���������������Mg2+��Fe3+
C. Ҫȷ������Һ�Ƿ���Na+����������ɫ��Ӧʵ�飬����ɫ�Ƿ�Ϊ��ɫ
D. ����Һ�п϶����е����ӵ����ʵ���֮��Ϊn��H+����n��NH4+����n��Al3+����n��SO42����=2��3��1��4
���𰸡�D
����������ͼ��֪����ʼ����NaOHû�г����������������һ����H+�����ʵ�����0.2mol�������г��������������ʧ����һ��û��Mg2+��Fe3+��һ������Al3+���м�γ������������䣬ӦΪNH4++OH-=NH3H2O�ķ�Ӧ������NH4+�����ʵ�����0.3mol���ܽ�����������������������0.1mol������������0.1mol���ɵ���غ��֪һ������SO42-�����������Ӳ���ȷ����������������ʵ�����(0.2+0.1��3+0.3)mol/2��0.4mol����A. �������Ϸ�����֪����Һ�п϶����е�������H+��NH4+��Al3+��SO42����A��ȷ��B. �϶���������������Mg2+��Fe3+��B��ȷ��C. Ҫȷ������Һ�Ƿ���Na+����������ɫ��Ӧʵ�飬����ɫ�Ƿ�Ϊ��ɫ��C��ȷ��D. ����������ʵ�������ȷ�������ܼ������ӵ����ʵ���֮�ȣ�D��������ѡD��


 ȫ�̽��ϵ�д�
ȫ�̽��ϵ�д� ����5��2���ϵ�д�
����5��2���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ұ��������Լ������б��淽����������������ȷ���� (����)
��� | �Լ� | ���淽�� | ���� |
A | ���� | ������ú���� | ��ֹ�������ˮ�������Ӵ�������Ӧ |
B | Һ�� | �ܷⱣ����ϸ��ƿ�� | ��ֹ���� |
C | ��ˮ | �����ĥ�ڲ���������ɫƿ�� | �������ֽ� |
D | ����� | �����ĥ�ڲ������Ĺ��ƿ�� | ��ֹ�ӷ� |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������β���е���Ҫ��Ⱦ����NO��NO2��CO��Ϊ���������Ⱦ���������ͨ�����·�Ӧ����������β����
[�о�һ]��NaOH��Һ����NO��NO2��
�ŵ�n(NO)�sn(NO2)=1ʱֻ����һ���Σ������εĻ�ѧʽΪ__________
�Ƶ�ֻ��NO2ʱ�����������Σ�2NO2+2NaOH=NaNO2+NaNO3+H2O����NaOH��Һǡ����ȫ����NO2����Һ�Լ��ԣ�����Һ������Ũ���ɴ�С��˳���ǣ�___________��
[�о���]һ��������CO��NOת��Ϊ����Ⱦ���2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) ��H
2CO2(g)+N2(g) ��H
����֪��2C(s)+O2(g)��2CO(g)����H1=��221.0KJ/mol
C(s)+O2(g)��CO2(g)����H2=��393.5KJ/mol
N2(g)+O2(g)��2NO(g)����H3=��180.5KJ/mol��
���H=______
��T���£��ڹ̶��ݻ����ܱ������У�ͨ��һ����NO��CO�������崫������ò�ͬʱ��NO��CO��Ũ�����±���
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO) 104 mol/L | 10.0 | 4.50 | 2.00 | 1.50 | 1.00 | 1.00 |
c(CO) 103 mol/L | 3.60 | 3.05 | 2.80 | 2.75 | 2.70 | 2.70 |
�ٸ������£�2s��N2��ƽ����Ӧ����v(N2)=_____________
�����������м���һ������ʯ�ң�COƽ��ת����_____��ѡ���������С�����䡱��
�������������䣬ֻ�ʵ������¶ȣ���4sʱ��c(NO)=c1mol/L����c1������_______
a��1.10��10��3 b��1.25��10��4 c��1.00��10��4 d��9.00��10��5
���о������ⶨ����β����CO�ĺ���
����CO�����Dzⶨ���÷����ǵĹ���ԭ��������ȼ�ϵ�أ����е�������ܴ���O2����Y2O3��ZrO2���壬�����ĵ缫��ӦʽΪ____________��
�������������⣨I2O5����������������⣺I2O5+5CO��I2+5CO2
��ȡ10L����β����������I2O5���գ�Ȼ�����100mL��Һ����ȡ���е�20.00mL��Һ����0.0050mol/LNa2S2O3��Һ�ζ�������ƽ��ʵ��ƽ������Na2S2O3��Һ�����Ϊ20.0mL����֪��2Na2S2O3+I2=Na2S4O6+2NaI����β����c(CO)=___________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����෨��һ����֮��Ч�������еĿ�ѧ��������������ʶ����ʱ���Բ�ȡ���ַ�����Բ��䵥һ���෨�IJ��㡣���й�����K2SO4���ķ���������
A������������
B������������
C�����ڼ���
D�����ڵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E��F���ֶ���������Ԫ�أ�ԭ������������������B�ĵ����ڳ�����Ϊ˫ԭ�ӷ��ӣ�����A�ĵ��ʿ��γɷ���X��X��ˮ��Һ�ʼ��ԣ�D�ļ���������X������ͬ����������D��ͬ�����м����Ӱ뾶��С��Ԫ�أ�EԪ�ص�ԭ�������ȴ�������������ӣ�C��F����Ԫ�ص�ԭ������㹲��13�����ӡ���
(1)A��Ԫ�ط���______________��D��Ԫ������ ____________��
(2)C�����ڱ��е�λ��Ϊ��______����______�壬E�����ӽṹʾ��ͼ________��
(3)B��C��E�ֱ���A�γɵĻ����������ȶ�����________(д��ѧʽ)��E��F������������Ӧ��ˮ��������Խ�ǿ����________(д��ѧʽ)
(4)F�ĵ����ڷ�Ӧ�г������������õ��ʵ�ˮ��Һ��E�ĵͼ������ﷴӦ�����ӷ���ʽΪ________________��
(5)X�ڴ�����C�����п�������ȼ�գ�����B�ĵ��ʡ��÷�Ӧ�Ļ�ѧ����ʽΪ��__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪������4�֣��ݴ˲�����д�������ж�C5H10O��ȩӦ��( )
A. 3�� B. 4�� C. 5�� D. 6��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ��D2O������Ҫ�ĺ˹�ҵԭ�ϣ�����˵��������ǣ� ��
A. 뮣�D��ԭ�Ӻ�����1������ B. 1H��D����ͬλ��
C. H2O��D2O����ͬ�������� D. 1H218O��D216O����Է���������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z���ֶ�����Ԫ�أ�ԭ�Ӱ뾶�Ĵ�С��ϵΪ��r(Y)>r(X)>r(Z)��ԭ������֮��Ϊ16��X��Y��Z����Ԫ�صij����������ʵ������¿ɷ�����ͼ��ʾ�仯������B��C��Ϊ10���ӷ��ӡ�����˵������ȷ����
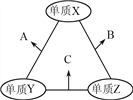
A. XԪ��λ����A��
B. A������B��
C. A��C�����ܷ���������ԭ��Ӧ
D. B�ķе����C�ķе�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com