
【题目】亚铁氰化钾的化学式为K4[Fe(CN)6],一种用含NaCN废水合成该化合物的主要工艺流程如图:

请依据工艺流程图中的信息,回答下列问题:
①在“除杂”步骤中弃渣的主要成分为________(填化学式)。
②在“反应器”中发生的主要反应的化学方程式为_______________________。
③相同温度下溶解度:Na4[Fe(CN)6]________K4[Fe(CN)6](填“>”“<”或“=”)。
【答案】CaCO3 6NaCN+FeSO4+CaCl2=CaSO4↓+Na4[Fe(CN)6]+2NaCl >
【解析】
根据题意可知,本题考查制备无机物的工艺流程,运用氧化氧还原反应规律和难溶电解质的转化规律分析。
①NaCN和FeSO4、CaCl2加入反应器后过滤得到弃渣CaSO4,滤液最后得到K4Fe(CN)6,说明反应器中还生成Na4Fe(CN),根据元素守恒知还生成NaCl,向滤液中加入Na2CO3,得到更难溶的CaCO3,
故答案为:CaCO3;
②NaCN和FeSO4、CaCl2加入反应器后过滤得到弃渣CaSO4,还生成Na4Fe(CN),根据元素守恒知还生成NaCl,因此在“反应器”中发生的主要反应的化学方程式为6NaCN+FeSO4+CaCl2=CaSO4↓+Na4[Fe(CN)6]+2NaCl;
故答案为;6NaCN+FeSO4+CaCl2=CaSO4↓+Na4[Fe(CN)6]+2NaCl;
③在转化罐中加入KCl溶液,过滤、洗涤、干燥得到K4[Fe(CN)6],说明在转化罐中发生反应,溶解度大的Na4[Fe(CN)6]转化为溶解度较小的K4[Fe(CN)6],
故答案为:>。


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
【题目】一定温度下的某容积不变的密闭容器中,建立下列化学平衡 C(s)+H2O(g)![]() CO(g)+H2(g),下列叙述中不能说明上述可逆反应已达到化学平衡状态的是
CO(g)+H2(g),下列叙述中不能说明上述可逆反应已达到化学平衡状态的是
A.体系的压强不再发生变化B.气体密度不再改变
C.生成n mol CO的同时生成n mol H2D.1 mol H–H键断裂的同时断裂2 molH–O键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据2CrO42﹣+2H+ ![]() Cr2O72﹣+H2O设计如图丙装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图丙中右侧电极连接电源的_________极,电解制备过程的总反应方程式为_________。测定阳极液中Na和Cr的含量,若Na与Cr的物质的量之比为a:b,则此时Na2CrO4的转化率为_________。若选择用熔融K2CO3作介质的甲醇(CH3OH)燃料电池充当电源,则负极反应式为________________。
Cr2O72﹣+H2O设计如图丙装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图丙中右侧电极连接电源的_________极,电解制备过程的总反应方程式为_________。测定阳极液中Na和Cr的含量,若Na与Cr的物质的量之比为a:b,则此时Na2CrO4的转化率为_________。若选择用熔融K2CO3作介质的甲醇(CH3OH)燃料电池充当电源,则负极反应式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钒(V)及其化合物有着广泛的用途。请回答下列问题:
(1)钒在溶液中的主要聚合状态与溶液的pH关系如图1所示。V2O74-中V元素的化合价是________,溶液中VO3-转化为V2O74-的离子方程式为________。

(2)偏钒酸铵是最普通的钒酸盐,将V2O5溶于碳酸钠溶液中(有气体生成),然后加入氯化铵,便可析出偏钒酸铵(NH4VO3),该过程总反应的化学方程式为________;当pH超过8.0时偏钒酸铵会发生转化,其原因是溶液中的VO3-转化为V2O74-、________(请另写出一点原因)。
(3)NH4VO3在高温下分解产生的V2O5可作为硫酸工业中2SO2(g)+O2(g)![]() 2SO3(g)ΔH=pkJ/mol反应的催化剂,其催化原理如图2所示。
2SO3(g)ΔH=pkJ/mol反应的催化剂,其催化原理如图2所示。

①过程a和过程b的热化学方程式为
V2O5(s)+SO2(g)=V2O4(s)+SO3(g) ΔH=qkJ/mol
V2O4(s)+O2(g)+2SO2(g)=2VOSO4(s) ΔH=rkJ/mol
则过程c的热化学方程式为_________。
②T℃时反应2SO3(g)![]() 2SO2(g)+O2(g) ΔH>0中SO3的转化率(α)与体系总压强(p)的关系如图3所示。T℃时,将2molSO3置于10L密闭容器中,反应达到平衡后,体系总压强为0.10MPa。则T℃时B点的化学平衡常数Kc=_________。
2SO2(g)+O2(g) ΔH>0中SO3的转化率(α)与体系总压强(p)的关系如图3所示。T℃时,将2molSO3置于10L密闭容器中,反应达到平衡后,体系总压强为0.10MPa。则T℃时B点的化学平衡常数Kc=_________。

(4)全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如图4所示。
①充电过程中,右槽溶液颜色逐渐由________色变为________色;
②充电时若转移的电子数为NA个,则左槽溶液中n(H+)的变化量为______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中,正确的是
A.甲烷的燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ·mol-1
B.500℃、30MPa下,将0.5molN2(g)和1.5molH2(g)置于密闭容器中充分反应生成NH3(g)放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g)△H=-38.6kJ·mol-1
2NH3(g)△H=-38.6kJ·mol-1
C.HCl和NaOH反应的中和热△H=-57.3kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ·mol-1
D.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(1)△H=-571.6kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨法溶浸氧化锌烟灰制取高纯锌的工艺流程如图所示。溶浸后氧化锌烟灰中锌、铜、镉、砷元素分别以[Zn(NH3)4]2+、[Cu(NH3)4]2+、[Cd(NH3)4]2+、[AsCl5]2-的形式存在。
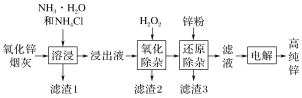
“氧化除杂”中,[AsCl5]2-转化为As2O5胶体吸附聚沉除去,溶液始终接近中性,该反应的离子方程式为_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,2.24LCl2通入NaOH溶液中反应转移的电子数为0.2NA
B. 常温下,1LpH=11的NaOH溶液中由水电离出的H+的数目为10-11NA
C. 273K、101kPa下,22.4L由NO和O2组成的混合气体中所含分子总数为NA
D. 100g34%双氧水中含有H-O键的数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用燃烧法测定某种氨基酸(CxHyOzNm)的分子组成。取Wg该种氨基酸放在纯氧中充分燃烧,生成二氧化碳、水和氮气。按下图所示装置进行实验。

回答下列问题:
(1)实验开始时,首先通入一段时间的氧气,其理由是__________________。
(2)以上装置中需要加热的仪器有_______ (填写字母),操作时应先点燃_____处的酒精灯。
(3)A装置中发生反应的化学方程式是____________________________。
(4)D装置的作用是____________________________。
(5)读取氮气的体积时,应注意①_________________;②_________________。
(6)实验中测得氮气的体积为VmL(标准状况),为确定此氨基酸的分子式,还需要的有关数据有____________________。
A.生成二氧化碳气体的质量
B.生成水的质量
C.通人氧气的体积
D.氨基酸的相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬及其化合物常被应用于冶金、化工、电镀、制药、纺织等行业,但使用后的废水因其中含高价铬的化合物而毒性很强,必须进行处理。工业上往往采取下列循环工艺防止铬的污染:
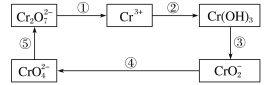
(1)上述各步反应中属于氧化还原反应的是__________(填序号)。
(2)第①步,含![]() 的废水在酸性条件下用绿矾FeSO4·7H2O处理,写出该反应的离子方程式:_________。
的废水在酸性条件下用绿矾FeSO4·7H2O处理,写出该反应的离子方程式:_________。
(3)第②步,向上述反应后的溶液中加入适量的碱石灰,使铬离子转变为Cr(OH)3沉淀。处理后,沉淀物中除了Cr(OH)3外,还有_____、____(写化学式)。已知Cr(OH)3性质类似Al(OH)3,是既能与强酸反应又能与强碱反应的两性物质,从沉淀中分离出Cr(OH)3的流程如图:
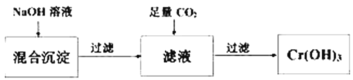
写出从该沉淀物中分离出Cr(OH)3的离子方程式__________、____________。
(4)回收所得的Cr(OH)3,经③④⑤步处理后又可转变成K2Cr2O7。纯净的K2Cr2O7常用于准确测定Na2S2O3溶液的物质的量浓度,方法如下:
①![]() +6I-+14H+=3I2+2Cr3++7H2O
+6I-+14H+=3I2+2Cr3++7H2O
②2![]() +I2=
+I2=![]() +2I-
+2I-
准确称取纯净的K2Cr2O7 0.1225g配成溶液,用上述方法滴定,消耗Na2S2O3溶液25.00mL。则Na2S2O3溶液的物质的量浓度为______(保留四位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com