
【题目】标明下列反应电子转移情况,并根据要求回答问题。
(1)3NO2+H2O=2HNO3+NO_______
(2)氧化剂____________还原剂____________氧化产物____________还原产物__________
科目:高中化学 来源: 题型:
【题目】I.已知:![]()
烃基烯基醚A的相对分子质量(Mr)为176,分子中碳氢原子数目比为3:4,与A相关的反应如下:

请回答下列问题:
(1)A的分子式为__,B的名称是__;
(2)写出C→D反应的化学方程式:__;
(3)链烃M的相对分子质量比B多24,分子中所有碳原子均在同一平面上,其结构简式是__;
Ⅱ.由E转化为对甲基苯乙炔(![]() )的一条路线如下:
)的一条路线如下:

(4)①反应中所加试剂是__; ③的反应类型是__;
(5)写出G的结构简式:__;
(6)写出两种同时符合下列条件的E的同分异构体的结构简式:__。
①属于芳香醛;
②苯环上有两种不同环境的氢原子.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在1L的烧瓶中充入一定量N2O4气体。
(1)体系中气体颜色由浅变深,写出对应的化学方程式____________________。
(2)保持温度和容积不变,向达到平衡的容器中再充入一定量N2O4气体,平衡________移动(填“正向”、“逆向”或“不”),N2O4的转化率___________(填“增大”、“减小”或“不变”,下同),反应的平衡常数___________。
(3)某小组为研究温度对化学平衡移动的影响,设计如图实验。图方案还需补充的是_____________(用文字表达);实验现象为______________________。

(4)在一定条件下,N2O4和NO2的消耗速率与压强关系为:v(N2O4)=k1·c(N2O4),v(NO2)=k2·c(NO2),设达到平衡时c(N2O4)=1 mol/L,则(1)中反应的平衡常数为_________(用k1、k2表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各图为几种晶体或晶胞的构型示意图。


请回答下列问题:
(1)这些晶体中,粒子之间以共价键结合形成的晶体是_______________。
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为_________。
(3)NaCl晶胞与MgO晶胞相同,NaCl晶体的晶格能________(填“大于”或“小于”)MgO晶体的晶格能,原因是__________________________。
(4)每个Cu晶胞中实际占有________个Cu原子,CaCl2晶体中Ca2+的配位数为________。
(5)冰的熔点远高于干冰的重要原因是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】银精矿(其化学成分有:Ag、Zn、Cu、Pb、S 及 SiO2 等)从其中提取银及铜和铅的工艺流程如图:

回答下列问题:
(1)“浸取”时,当盐酸的浓度和 KClO3 的量一定时,为提高浸取率可采取的措施是______(请用简练语言列举一项)。
(2)“分离Ⅰ”所加试剂 X 为______,“分离Ⅱ”所得滤渣中除含单质硫外,还含有的成分有______。
(3)“浸银”反应的化学方程式为______
(4)N2H4 的电子式为______,“还原”反应的离子方程式为______。
(5)“粗银”(含 Ag、Cu、Zn、Au)可用立式电解槽电解精炼,纯银作阴极,电解液采用硝酸和硝酸银的混合溶液。硝酸浓度不能过大,其原因是______(写出一条即可)。
(6)此类工厂排出的废水中含有 NO3-,对人体有害。科技人员在碱性条件下用 Al 粉将 NO3-还原为 N2。缺点是处理后的水中引入了 AlO2-,仍然对人体健康有害。
已知:25℃时,Ksp[Al(OH)3]=1.3×10-33 Al(OH)3H+ + AlO2- + H2O K=1.0×10-13
①25℃时,欲将上述处理过水中的 AlO2- 浓度降到 1.0×10-6 mol/L,此时水中 c(Al3+)=______mol/L。
②25℃时,Al(OH)3 溶于 NaOH 溶液反应的平衡常数 K=______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今年是门捷列夫发现元素周期律150周年。下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法不正确的是
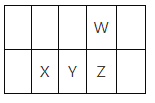
A.原子半径:W<XB.常温常压下,Y单质为固态
C.最高价氧化物对应水化物的酸性:Y<ZD.X的最高价氧化物的水化物是强碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL 0.1mol·L-1氨水中滴加某浓度的硫酸溶液,溶液中水电离的c(H+)随加入硫酸的体积变化如图所示。下列说法不正确的是

A.若a点对应水电离的c(H+)=1.0×10-11mol·L-1,则此时氨水的电离程度为1%
B.c点时氨水与硫酸恰好完全反应
C.c点对应溶液中:c(H+)-c(OH-)=c(NH3·H2O)
D.若b、d点对应水电离的c(H+)=1.0×10-7mol·L-1,则两溶液中均存在:c(NH4+)=2c(SO42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】佛罗那可用于治疗新生儿高胆红素血症。以甲苯为原料制备佛罗那的合成路线如图:
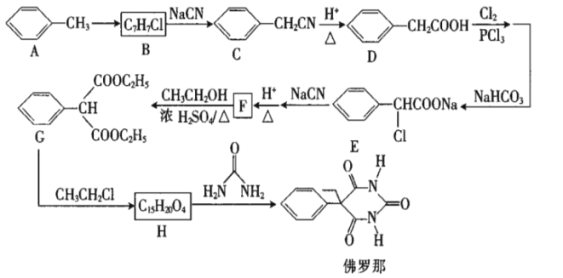
回答下列问题:
(1)D的名称是__,B中官能团的名称为__。
(2)写出H的结构简式:__。
(3)结构中不含碳碳双键,有六个碳原子在同一条直线上的B的同分异构体的结构简式有__种(不考虑立体异构),写出其中一种结构的结构简式:__。
(4)上述合成路线中有字母代号的物质中有手性碳原子的是__(填字母代号)。(已知:连有四个不同的原子或原子团的碳原子称为手性碳原子)
(5)H→佛罗那的反应类型为__。
(6)写出F→G的化学方程式:__。
(7)参照上述合成路线,设计以丙二酸、乙醇和氯乙烷为原料合成乙基丙二酸的合成路线__(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期主族元素![]() 和W的原子序数依次增大,X和Y的单质化合生成气体A,A分子中的电子数与氖原子相同,X和W的单质化合生成气体B,常温下
和W的原子序数依次增大,X和Y的单质化合生成气体A,A分子中的电子数与氖原子相同,X和W的单质化合生成气体B,常温下![]() 的B溶液的
的B溶液的![]() ,气体A和气体B相遇产生白烟,X与Z可按原子个数比1∶1形成化合物C。下列说法正确的是( )
,气体A和气体B相遇产生白烟,X与Z可按原子个数比1∶1形成化合物C。下列说法正确的是( )
A.化合物C可能为离子化合物
B.Z离子的半径比Y离子的大
C.Y的非金属性很强,其单质非常活泼
D.氧化物的水化物的酸性:Y比W强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com