
【题目】(1)下列物质中,既含离子键又含共价键的化合物是_________;同时存在σ键和π键的分子是_________,含有极性键的非极性分子是_________。
A.N2 B.C2H6 C.CaCl2 D.NH4Cl
(2)用“>”或“<”填空:
晶格能:Na2O_______KCl 酸性:H2SO4_______HClO4 离子半径:Al3+_______F-
【答案】D A B > < <
【解析】
(1)A.N2分子含有非极性共价键,属于单质,氮气分子结构简式为N≡N,所以氮气分子中含有σ键和π键的非极性分子;
B.C2H6分子中碳原子和氢原子之间存在极性键,碳原子和碳原子之间存在非极性共价键,属于共价化合物,乙烷的结构式为![]() ,乙烷分子中只含σ键的非极性分子;
,乙烷分子中只含σ键的非极性分子;
C.CaCl2中只含离子键,属于离子化合物;
D.NH4Cl中铵根离子和氯离子之间存在离子键,氮原子和氢原子之间存在共价键,属于离子化合物,铵根离子中氮原子和氢原子之间存在σ键;
(2)离子化合物中,阴阳离子半径越小,离子所带电荷数越多,晶格能越大;非金属性越强,所对应元素的最高价含氧酸的酸性越强;具有相同电子排布的离子中,原子序数大的离子半径小。
(1)由分析可知:既含离子键又含共价键的化合物是NH4Cl;同时存在σ键和π键的分子是N2;含有极性键的非极性分子是C2H6。
(2)Na+的半径比K+半径小,O2-的半径比Cl-半径小,并且O2-带的电荷数比Cl-多,故晶格能:Na2O>KCl;
同周期从左向右非金属性增强,非金属性S<Cl,对应最高价含氧酸的酸性为H2SO4< HClO4;
具有相同电子排布的离子中,原子序数大的离子半径小,则离子半径为Al3+< F-。


科目:高中化学 来源: 题型:
【题目】β—紫罗兰酮是存在于玫瑰花、番茄等中的一种天然香料,它经多步反应可合成维生素A1。下列说法正确的是( )
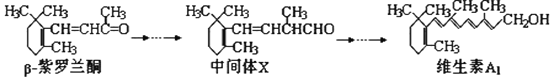
A. β—紫罗兰酮与中间体X互为同分异构体
B. β—紫罗兰酮不可使酸性KMnO4溶液褪色
C. 维生素A1易溶于NaOH溶液
D. 1mol维生素A1最多能与5molH2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)![]() 的名称为______________________。
的名称为______________________。
(2)A,B,C三种烃的化学式均为C6H10,它们的分子中均无支链或侧链。
①若A为环状,则其结构简式为_________________________________。
②若B为含有双键的链状结构,且分子中不存在“![]() ”基团,则其可能的结构简式为_______(任写一种)。
”基团,则其可能的结构简式为_______(任写一种)。
③若C为含有三键的链状结构,则其可能的结构简式及名称为__________。
(3)下列是八种环状的烃类物质:
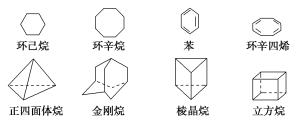
①互为同系物的有________和________(填名称),互为同分异构体的有________和________,________和________(填写名称,可以不填满,也可以再补充)。
②正四面体烷的二氯取代产物有________种;立方烷的二氯取代产物有________种;金刚烷一氯取代产物有________种。
③写出与苯互为同系物且一氯代物只有两种的物质的结构简式(举两例)并用系统命名法命名:___________________________________________。
(4)今有三种化合物结构如下:
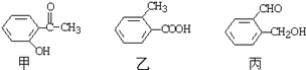
①请写出丙中含氧官能团的名称:__________________________________;
②请判断上述哪些化合物互为同分异构体:_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是

A. 向圆底烧瓶中滴加苯和溴的混合液前需先打开K
B. 实验中装置b中的液体逐渐变为浅红色
C. 装置c中的碳酸钠溶液的作用是吸收溴化氢
D. 反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设 NA 为阿伏加德罗常数的值,下列说法正确的是
A.某密闭容器中盛有 0.1molN2 和 0.3molH2,在一定条件下充分反应,转移电子的数目为 0.6NA
B.常温下,1L pH=9 的 CH3COONa 溶液中,发生电离的水分子数为 1×109 NA
C.14.0gFe 发生吸氧腐蚀生成 Fe2O3xH2O,电极反应转移的电子数为 0.5NA
D.标准状况下,2.24L 丙烷含有的共价键数目为 1.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Al、Ti、Co、Cr、Zn 等元素形成的化合物在现代工业中有广泛的用途。回答下列问题:
(1)下列状态的铝中,电离最外层的一个电子所需能量最小的是_____(填标号)。
A.[Ne]3s1 B.[Ne]3s2 C.[Ne]3s23p1 D.[Ne] 3s13p2
(2)熔融 AlCl3 时可生成具有挥发性的二聚体 Al2Cl6,二聚体 Al2Cl6 的结构式为_____;(标出配位键)其中 Al 的配位数为_________。
(3)与钛同周期的所有副族元素的基态原子中,最外层电子数与基态钛原子相同的元素有_____种。
(4)Co2+的价电子排布式_________。NH3 分子与 Co2+结合成配合物[Co(NH3)6]2+,与游离的氨分子相比,其键角∠HNH_____(填“较大”,“较小”或“相同”),解释原因_____。
(5)已知 CrO5 中铬元素为最高价态,画出其结构式:_____。
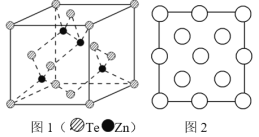
(6)阿伏加德罗常数的测定有多种方法,X 射线衍射法就是其中的一种。通过对碲化锌晶体的 X 射线衍射图 象分析,可以得出其晶胞如图 1 所示,图 2 是该晶胞沿 z 轴的投影图,请在图中圆球上涂“●”标明 Zn 的位置_____。若晶体中 Te 呈立方面心最密堆积方式排列,Te 的半径为 a pm,晶体的密度为 ρg/cm3,阿伏加德罗常数 NA=_____mol-1(列计算式表达)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学课外兴趣小组为了探究影响化学反应速率的因素,做了以下实验。
(1)用三支试管各取5.0 mL、0.01 mol·L-1的酸性KMnO4溶液,再分别滴入0.1 mol·L-1 H2C2O4溶液,实验报告如下。

①实验1、3研究的是_________对反应速率的影响。
②表中V=_________mL。
(2)小组同学在进行(1)中各组实验时,均发现该反应开始时很慢,一段时间后速率会突然加快。对此该小组的同学展开讨论:
①甲同学认为KMnO4与H2C2O4的反应放热,温度升高,速率加快。
②乙同学认为随着反应的进行,因_________,故速率加快。
(3)为比较Fe3+、Cu2+对H2O2分解的催化效果,该小组的同学又分别设计了如图甲、乙所示的实验。回答相关问题:

①装置乙中仪器A的名称为_________。
②定性如图甲可通过观察反应产生气泡的快慢,定性比较得出结论。有同学提出将CuSO4溶液改为CuCl2溶液更合理,其理由是____________________________________。
③定量如图乙所示,实验时以收集到40 mL气体为准,忽略其他可能影响实验的因素,实验中需要测量的数据是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是由4个碳原子结合成的4种有机物(氢原子没有画出)

(1)写出有机物(a)的系统命名法的名称________。
(2)有机物(a)有一种同分异构体,试写出其结构简式________。
(3)上述有机物中与(c)互为同分异构体的是________(填代号)。
(4)任写一种与(e)互为同系物的有机物的结构简式________________。
(5)上述有机物中4个碳原子处于同一平面的有________(填代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物浆液含Al(OH)3、MnO2和少量Na2Cr2O4。考虑到胶体的吸附作用使Na2Cr2O4不易完全被水浸出,某研究小组利用设计的电解分离装置(如图1),使浆液分离成固体混合物和含铬元素溶液,并回收利用。
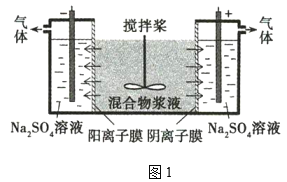
固体混合物的分离和利用的流程图如图2所示(流程图中的部分分离操作和反应条件未标明):
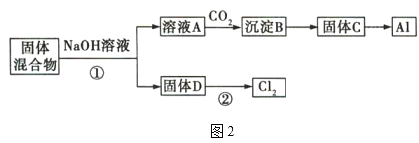
(1)反应①所加试剂NaOH的电子式为___,B→C的反应条件为___,C→Al的制备方法称为___。
(2)该小组探究反应②发生的条件。D与浓盐酸混合,不加热,无变化;加热有Cl2生成,当反应停止后,固体有剩余,此时滴加硫酸,又产生Cl2。由此判断影响该反应有效进行的因素有___(填序号)。
a.温度 b.Cl-的浓度 c.溶液的酸度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com