
分析 将原子核内所有的质子和中子的相对质量取近似整
数值加起来所得的数值,叫做质量数,
将原子核内所有的质子和中子的相对质量取近似整
数值加起来所得的数值,叫做质量数,
根据质量数是如果忽略电子的质量,将原子核内所有质子和中子的相对质量取近似整数值加起来,所得的数值.用符号A表示.即:质量数=质子数+中子数,原子符号ZAX中Z表示质子数,A表示质量数,X表示元素符号.
解答 解:将原子核内所有的质子和中子的相对质量取近似整数值加起来.所得的数值,叫做质量数,用符号A表示.质子数用Z表示,则原子X可表示为ZAX;
故答案为:质量数;A;Z;ZAX;
点评 本题考查了原子结构和性质,题目难度不大,注意把握原子的构成以及微粒之间的关系.


 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源: 题型:选择题
| 物质 | H2CO3 | HClO | HAlO2 |
| 电离常数 (25℃) | Ka1=4.4×10-7 | Ka=3×10-8 | Ka=6.3×10-13 |
| Ka2=4.7×10-11 |
| A. | NaClO溶液中通入过量CO2:ClO-+CO2+H2O═HClO+HCO3- | |
| B. | NaClO溶液中通入少量CO2:2ClO-+CO2+H2O═2HClO+CO32- | |
| C. | NaAlO2溶液中加入过量CO2:AlO2-+CO2+2H2O═HCO3-+Al(OH)3↓ | |
| D. | NaAlO2溶液中通入少量CO2:2AlO2-+CO2+3H2O═CO32-+2Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a与其他元素生成的化合物都是离子化合物 | |
| B. | b与氢形成的所有化合物中化学键均为极性共价键 | |
| C. | c存在两种或两种以上的氧化物 | |
| D. | 在四种元素中,d元素的非金属性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
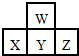 如图是周期表中短周期的一部分.若X原子最外层电子数比次外层电子数少3个,则下列说法中不正确的是( )
如图是周期表中短周期的一部分.若X原子最外层电子数比次外层电子数少3个,则下列说法中不正确的是( )| A. | 原子半径的大小顺序是Z>Y>X>W | |
| B. | Z的气态氢化物比X的气态氢化物稳定 | |
| C. | X、Y、Z各元素最高价和最低价的绝对值之和为8 | |
| D. | X、Y、Z最高价氧化物对应水化物的酸性强弱关系Z>Y>X |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 加入试剂 | 对应化学或离子方程式 | ||
| A | 乙烷(乙烯) | 氢气 | CH2=CH2+H2$→_{加热}^{Ni}$CH3CH3 |
| B | CH3COOC2H5(CH3COOH) | NaOH溶液 | CH3COOH+NaOH=CH3COONa+H2O |
| C | MgCl2( FeCl3) | 氨水 | Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+ |
| D | Fe2+(Fe3+) | Fe粉 | 2Fe3++Fe=3Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16O与18O互为同位素;H216O、D216O、H218O、D218O互为同素异形体 | |
| B. | SiH4、PH3、HCl的稳定性逐渐增强 | |
| C. | 乙烯的结构简式CH2CH2 | |
| D. | Ca2+的结构示意图为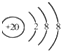 NH4Cl的电子式为 NH4Cl的电子式为 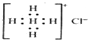 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com