
25℃时,溶液只含有Na+、H+、OH-、CH3COO-这四种离子,下列说法错误的是
A.溶液只能是CH3COONa溶液
B.溶液中的离子浓度可能是c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
C.溶液中的离子浓度可能是c(Na+)> c(CH3COO-)> c(OH-)>c(H+)
D.溶液中的离子浓度可能是c(Na+)> c(OH-)> c(CH3COO-)> c(H+)
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015陕西省高一下学期第一次月考化学试卷(解析版) 题型:选择题
根据元素周期律判断,下列递变规律不正确的是
A.Na、Mg、Al的金属性依次减弱
B.HCl、HBr、HI的稳定性依次增强
C.HClO4、H 2SO4、H3PO4的酸性依次减弱
2SO4、H3PO4的酸性依次减弱
D.Li、Na、K分别与水反应的剧烈程度依次增强
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁朝阳市三校协作体高三下学期第一次联考理综化学试卷(解析版) 题型:填空题
(12分)在右图均用石墨作电极的电解池中,甲池中为500mL含某一溶质的蓝色溶液,乙池中为500mL稀硫酸,闭合K1,断开K2进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,立即停止电解,取出A电极,洗涤、干燥、称量,电极质量增重1.6g。请回答下列问题:

(1)电解过程中,乙池C电极发生反应的电极反应式 。
(2)甲池电解时反应的离子方程式 。
(3)甲池电解后溶液的pH= ,要使电解后溶液恢复到电解前的状态,则需加入 ,
其质量为 g。(假设电解前后溶液的体积不变)
(4)电解后若再将K1断开,闭合K2,电流计指针发生偏转,则D电极发生反应的电极反应式 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省高三4月联考理综化学试卷(解析版) 题型:选择题
常温下,用0.1000mol/L的NaOH溶液滴定20ml同浓度的一元弱酸HA,滴定过程溶液pH随X的变化曲线如图所示(忽略中和热效应),下列说法不正确的是

A.HA溶液加水稀释后,溶液中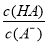 的值减小
的值减小
B.HA的电离常数 (x为滴定分数)
(x为滴定分数)
C.当滴定分数为100时,溶液中水的电离程度最大
D.滴定分数大于100时,溶液中离子浓度关系一定是c(Na+)>c(A-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年贵州省八校联盟高三第二次联考理综化学试卷(解析版) 题型:填空题
(14分)CO是水煤气的主要成份之一,是一种无色剧毒气体,根据信息完成下列各题
Ⅰ、已知下列热化学方程式
2C(s) + O2(g) = 2CO(g) △H = -221kJ/mol
C(s) + O2(g) = CO2(g) △H = -393kJ/mol
24g单质碳在不足量的O2中燃烧时,生成等物质的量的CO和CO2气体,则和24g单质碳完全燃烧生成CO2相比较,损失热量_________kJ
Ⅱ、850℃时,在10L体积不变的容器中投入2molCO和3molH2O,发生如下反应:
CO(g) + H2O(g)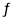 CO2(g) + H2(g)
CO2(g) + H2(g)
当CO的转化率达60%时,反应达平衡
(1)850℃时,该反应的平衡常数为_________
(2)该条件下,将CO和H2O都改为投入2mol,达平衡时,H2的浓度为_________mol/L,下列情况能说明该反应一定达平衡的是_________
A.CO和H2O蒸气的浓度之比不再随时间改变
B.气体的密度不再随时间改变
C.CO和CO2的浓度之比不再随时间改变
D.气体的平均摩尔质量不再随时间改变
Ⅲ、为防止CO使人中毒,一种CO分析仪的工作原理如图所示,该装置中电解质为氧化钇——氧化钠,其中O2-可以在固体NASICON中自由移动,则:

(1)该原电池中通入CO的电极为_________极,该电极的电极反应式为___________________
(2)通空气一极的电极反应式为____________________________________
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市朝阳区高三4月第一次综合练习理综化学试卷(解析版) 题型:实验题
(15分)某学生对Na2SO3与AgNO3在不同PH下的反应进行探究。
(1)测得Na2SO3溶液PH=11,AgNO3溶液PH=5,二者水解的离子分别是 。
(2)调节PH,实验记录如下:

查阅资料得知:
i.Ag2SO3:白色,难溶于水,溶于过量Na2SO3的溶液
ii.Ag2O:棕黑色,不溶于水,能和酸反应
①推测a中白色沉淀为Ag2SO3,离子方程式是 。
②推测a中白色沉淀为Ag2SO4,推测的依据是 。
(3)取b、c中白色沉淀,置于Na2SO3溶液中,沉淀溶解。该同学设计实验确认了白色沉淀不是Ag2SO4,实验方法是:另取Ag2SO4固体置于 溶液中,未溶解。
(4)将中滤出、洗净,为确认其组成,实验如下:
Ⅰ.向X中滴加稀盐酸,无明显变化
Ⅱ.向X中加入过量浓HNO3,产生红棕色气体
Ⅲ.用Ba(NO3)2溶液、BaCl2溶液检验Ⅱ中反应后的溶液,前者无变化,后者产生白色沉淀
①实验Ⅰ的目的是 。
②根据上述现象,分析X的性质和元素组成是 。
③Ⅱ中反应的化学方程式是 。
(5)该同学综合以上实验,分析产生X的原因,认为随着酸性的增强,还原性增强。通过进一步实验确认了这种可能性,实验如下:

①气体Y是 。
②白色沉淀转化为X的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高一下学期学期第一次月考化学试卷(解析版) 题型:选择题
任何科学真理的发现,都不是一帆风顺的,门捷列夫的元素周期表奠定了现代化学和物理学的理论基础。下列关于元素周期表的说法中,不正确的是
A.周期表中的副族、Ⅷ族都是金属元素
B.周期表中的ⅡA族都是金属元素
C.周期表中的非金属元素都位于短周期
D.周期表中的0族元素都是非金属元素
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省分校高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列反应中不需加热的吸热反应是
A.锌粒与稀硫酸的反应
B.灼热的木炭与CO2反应
C.甲烷在氧气中的燃烧反应
D.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com