
| A. | 水、四氯化碳、苯 | B. | AgNO3、NaOH、KI | C. | NaCl、NaBr、NaI | D. | 汽油、酒精、NaOH |
分析 溴水具有强氧化性,可与KI等溶液发生氧化还原反应,与NaOH溶液反应生成NaBr、NaBrO,易溶于有机物溶剂,以此解答该题.
解答 解:A.四氯化碳、苯都不溶于水,四氯化碳密度比水大,苯的密度比水小,可鉴别,故A正确;
B.溴水和AgNO3反应可生成AgBr浅黄色沉淀,溴水和NaOH溶液反应溴水褪色,溴水与KI反应可以置换出I2,溶液的由橙黄色变为棕黄色,颜色发生改变,故B正确;
C.溴水与NaCl、NaBr溶液都不反应,不能鉴别,故C错误;
D.溴水和汽油混合溶液会分层,和酒精互溶不分层,但溴水不褪色,溴水和NaOH溶液混合,不分层但溴水会褪色,故D正确,
故选C.
点评 本题考查物质的检验和鉴别,为高考常见题型和高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质的异同,注重基础知识的学习,难度不大.


科目:高中化学 来源: 题型:实验题
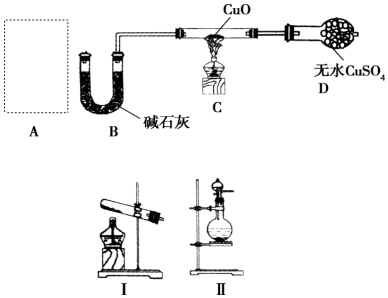
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将NO2通入水中,气体由红棕色逐渐转变为无色 | |
| B. | 向澄清的石灰水中通入SO2,有白色沉淀形成 | |
| C. | NH3使湿润的红色石蕊试纸变蓝 | |
| D. | 向Fe2(SO4)3溶液中滴加NaOH溶液,生成红褐色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 神舟九号升空时火箭发射的动力主要来源于化学能 | |
| B. | 洁厕灵的主要成分是盐酸,不能与“84”消毒液混用 | |
| C. | 采用催化转换技术将汽车尾气中的NOx和CO转化为无毒气体 | |
| D. | 高纯硅广泛应用于太阳能电池、计算机芯片和光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含碳元素的化合物都是有机物 | |
| B. | 苯的同系物能使KMnO4酸性溶液褪色 | |
| C. | 石油分馏可获得乙烯、丙烯和丁二烯 | |
| D. | 酯类和醇类均能发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
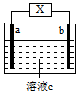
| A. | a、b不可能是同种材料的电极 | |
| B. | X为电流计,c为稀盐酸,该装置为原电池 | |
| C. | X为直流电源,c为稀硫酸,该装置为电解池 | |
| D. | X为电流计,c为稀硫酸,a可能为铜电极,b可能为锌电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.lmol Fe在0.lmolCl2中充分燃烧,转移的电子数为0.3NA | |
| B. | 25℃时,pH=13的1.0 LBa(OH)2溶液中含有的OH-数目为0.2NA | |
| C. | 含NA个氧原子的O2与含NA个氧原子的O3的质量比为2:3 | |
| D. | lmol CnH2n+2分子中含共价键数目为(3n+1)NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com