
| A�� | ��ȡ3.84g CuSO4��ĩ������250mLˮ | |
| B�� | ��ȡ6.25g CuSO4•5H2O���壬��ˮ���250mL��Һ | |
| C�� | ��ȡ4.0g CuSO4��ĩ������250mLˮ | |
| D�� | ��ȡ4.0g CuSO4•5H2O���壬��ˮ���250mL��Һ |
���� ʵ��������240mL 0.1mol•L-1������ͭ��Һ��ʵ�������Ƶ���250ml 0.1mol/L������ͭ��Һ����CuSO4��CuSO4•5H2O�����ʵ�����n��CuSO4��=n��CuSO4•5H2O��=0.1mol•L-1��0.25L=0.025mol��m��CuSO4��=0.025mol��160g•mol-1=4.0g��m��CuSO4•5H2O��=0.025mol��250g•mol-1=6.25g���ݴ˶Ը�ѡ������жϣ�
��� �⣺����240mL��Һ����Ҫʹ��250mL����ƿֻ������250mL��Һ������ͭ����������Һ�����ʶ���CuSO4����ȡ�κ�һ�ֶ����ԣ�
A������250mL��Һ�������������м���500mLˮ����A����
B��M��CuSO4��=160g•mol-1��M��CuSO4•5H2O��=250g•mol-1������250mL0.1mol•L-1CuSO4��Һ��CuSO4��CuSO4•5H2O�����ʵ�����n��CuSO4��=n��CuSO4•5H2O��=0.1mol•L-1��0.25L=0.025mol��m��CuSO4��=0.025mol��160g•mol-1=4.0g��m��CuSO4•5H2O��=0.025mol��250g•mol-1=6.25g����B��ȷ��
C�����Ƶ���250mL��Һ�������������м���500mLˮ����C����
D������B��֪��С�ڳ���6.25g4.0g CuSO4•5H2O���壬��D����
��ѡB��
���� ���⿼��������һ��Ũ�ȵ���Һ��������Ŀ�Ѷ��еȣ���ȷ�ж�������Һ���Ϊ���ؼ���ע����������һ�����ʵ���Ũ�ȵ���Һ����������������ѧ���ķ�����������ѧʵ��������


 ֱͨ������У�ܲ��¿�ֱͨ��Уϵ�д�
ֱͨ������У�ܲ��¿�ֱͨ��Уϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HCO3-+H+?H2CO3 | B�� | HCO3-+OH-�TH2O+CO32- | ||
| C�� | NH3+H+�TNH4+ | D�� | NH3•H2O?NH4++OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
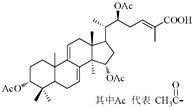 ij��У�о���������������ͼ���������֥�ᵥ��ķ��ӽṹͼ��ͼ��ʾ�����й��ڸ��л����˵������ȷ���ǣ�������
ij��У�о���������������ͼ���������֥�ᵥ��ķ��ӽṹͼ��ͼ��ʾ�����й��ڸ��л����˵������ȷ���ǣ�������| A�� | ����Br2�����ӳɷ�Ӧ | B�� | �ܷ���������Ӧ | ||
| C�� | �ܷ���ˮ�ⷴӦ | D�� | ��������7������̼ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
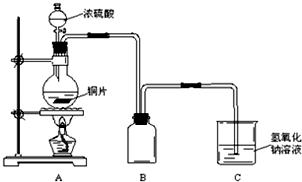
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| n��SO32-����n��HSO3-�� | 91��9 | 1��1 | 9��91 |
| pH | 8.2 | 7.2 | 6.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
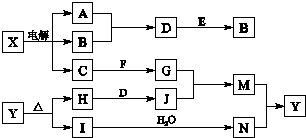
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢۢܢݢ� | B�� | �ۢܢڢ٢ޢ� | C�� | �٢ܢۢڢޢ� | D�� | �٢ۢܢڢޢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com