

| A、图①表示25℃时,用0.1 mol?L-1盐酸滴定20 mL 0.1 mol?L-1 KOH溶液,溶液的pH随加入酸体积的变化 |
| B、图②中曲线表示反应N2(g)+3H2(g)═2NH3(g)△H<0 正、逆反应的平衡常数K随温度的变化 |
| C、图③表示醋酸溶液滴定NaOH和氨水混合溶液的电导率曲线 |
| D、图④中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g);△H<0使用和未使用催化剂时,反应过程中的能量变化 |


科目:高中化学 来源: 题型:
| A、Fe3+、Na+、Cl-、SCN- | ||
B、HCO3-、Ca2+、C
| ||
| C、Na+、AlO2-、NO3-、H+ | ||
| D、K+、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
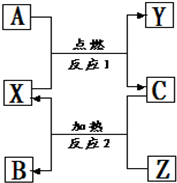 A、B、C是中学化学常见的单质,X、Y、Z是中学化学常见的氧化物,它们之间有如右图所示的转化关系,请据图回答:
A、B、C是中学化学常见的单质,X、Y、Z是中学化学常见的氧化物,它们之间有如右图所示的转化关系,请据图回答:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、2d | B、10d |
| C、5d | D、0.8d |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是某只含有C、H、O、N的有机物简易球棍模型.下列关于该有机物的说法正确的是( )
如图是某只含有C、H、O、N的有机物简易球棍模型.下列关于该有机物的说法正确的是( )| A、分子式为C3H7NO |
| B、在一定条件下,可以生成高分子化合物 |
| C、不能和盐酸溶液反应 |
| D、不能和NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,32克氧气中原子个数为NA |
| B、标准状况下,1mol H2O的体积为22.4L |
| C、常温常压下,1mol H2的质量为2克 |
| D、物质的量浓度为0.5mol/L的MgCl2溶液中,含有的Cl-数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | ② | ③ | ④ |
| 0.1mol?L-1氨水 | Ph=11 氨水 |
0.1mol?L-1 盐酸 |
pH=3 盐酸 |
| A、由水电离出的c(H+):③>① |
| B、①稀释到原来的100倍,pH与②相同 |
| C、①与③混合,若溶液pH=7,则溶液中c(NH4+)>C(Cl-) |
| D、②与④等体积混合,混合液pH>7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在①CO2、②NO2、③CO、④Cl2、⑤HCl、⑥NH3等气体中(选填序号)
在①CO2、②NO2、③CO、④Cl2、⑤HCl、⑥NH3等气体中(选填序号)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com