
| A.原溶液中溶质的质量为32g |
| B.电解过程中转移电子的物质的量为0.8mol |
| C.电解过程中阳极产生的气体在标准状况下的体积为4.48L |
| D.在相同条件下,阴极得到气体的体积大于阳极得到气体的体积 |
科目:高中化学 来源:不详 题型:填空题
| A.C(s)+H2O(g)==CO(g)+H2(g):△H>0 |
| B.Ba(OH)2·8H2O(s)+2NH4Cl(s)==BaCl2(aq)+2NH3·H2O(l)+8H2O(l)△H>0 |
| C.CaC2(s)+2 H2O(l)==Ca(OH)2(s)+C2H2(g);△H<0 |
| D.CH4(g)+2O2(g)==CO2(g)+2H2O(l):△H<0 |
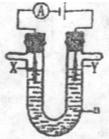
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
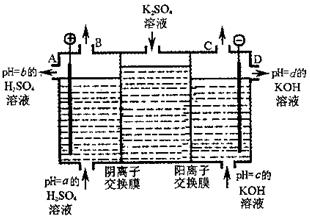
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
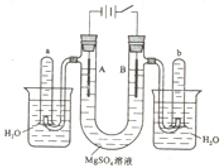
 ” 或“
” 或“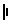 ”表示)、烧杯、灵
”表示)、烧杯、灵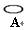 ”表示)和两个电极棒(分别是M、N)进行电化学实验探究。
”表示)和两个电极棒(分别是M、N)进行电化学实验探究。 象回答以下问题:
象回答以下问题: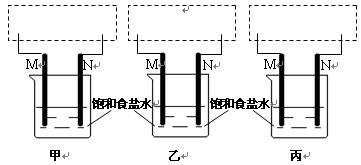
 。
。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 KCl + Na NaCl + K + Q (Q<0)
KCl + Na NaCl + K + Q (Q<0)| | 熔点℃ | 沸点℃ | 密度(g/cm3) |
| Na | 97.8 | 882.9 | 0.97 |
| K | 63.7 | 774 | 0.86 |
| NaCl | 801 | 1413 | 2.165 |
| KCl | 770 | 1500(升华) | 1.984 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Na2Sx,以下说法正确的是
Na2Sx,以下说法正确的是| A.放电时,Na作正极,S极发生还原反应 |
| B.若用此电池电解硝酸银溶液,当阴极上产生标准状况下气体1.12 L时,消耗金属钠2.3 g |
| C.充电时,钠极与外电源的正极相连 |
D.充电时,阳极发生的反应为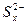  xS+2e- xS+2e- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.能自发进行的氧化还原反应,一般可以设计成原电池 |
| B.电解质溶液导电是化学变化,金属导电是物理变化 |
| C.电解池和原电池中均发生氧化还原反应 |
| D.电解、电离、原电池均需要通电 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.不溶性盐都是弱电解质,可溶性酸都是强电解质 |
| B.强酸溶液中的氢离子浓度一定大于弱酸溶液中的氢离子浓度 |
| C.二氧化硫和乙醇均属共价化合物,是非电解质 |
| D.NaOH溶液的导电性一定比氨水溶液的导电性强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 离子 | 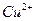 | 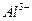 | 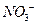 | 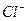 |
| 物质的量浓度(mol/L) | 1 | 1 | a | 1 |
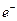 通过时(忽略电解时溶液体积的变化及电
通过时(忽略电解时溶液体积的变化及电| A.电解后溶液的pH="0" | B.a=3 |
C.阳极生成1.5 mol 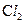 | D.阴极析出的金属是铜与铝 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com