
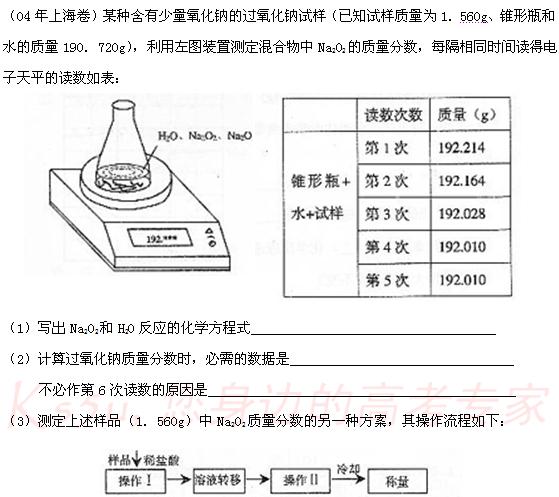
①操作Ⅱ的名称是
②需直接测定的物理量是
③测定过程中需要的仪器有电子天平、蒸发皿、酒精灯,还需要 、
(固定、夹持仪器除外)
④在转移溶液时,如溶液转移不完全,则Na2O2质量分数的测定结果
(填偏大、偏小或不变)。
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
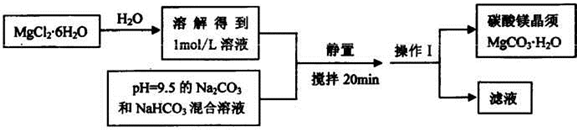
| 实验步骤 | 预期的实验现象和结论 |
| 取一定质量的固体样品 置于试管中,滴加足量的稀盐酸 (或置于试管中充分加热,将产生的气体通入到盛有足量澄清石灰水的烧杯) 置于试管中,滴加足量的稀盐酸 (或置于试管中充分加热,将产生的气体通入到盛有足量澄清石灰水的烧杯) |
若 无气泡生成 (或澄清石灰水不变浑浊 ) 无气泡生成 ,则固体产物为Mg(OH)2(或澄清石灰水不变浑浊 ) |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
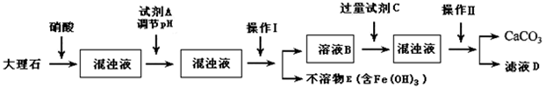
 ,溶液变红色,说明滤液中含Fe3+
,溶液变红色,说明滤液中含Fe3+ ,溶液变红色,说明滤液中含Fe3+
,溶液变红色,说明滤液中含Fe3+查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
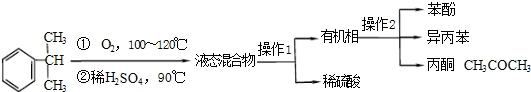
| 物质 | 沸点 | 溶解性 | 主要化学性质 |
| 异丙苯 | 152.4℃ | 不溶于水,易溶于酒精. | 可被强氧化剂氧化 |
| 苯酚 | 181.8℃ | 微溶于冷水,易溶于热水和酒精等有机溶剂. | 易被氧化 |
| 丙酮 | 56.2℃ | 易溶于水和有机溶剂 | 不易被氧化 |
| 检验项目 | 实验方案 |
| 检验丙酮中一定存在有机杂质的方法是 A A |
A.酸性KMnO4溶液,加热 B.乙醇,溶解 C.NaOH溶液(酚酞),加热 |
| 检验丙酮中一定含有苯酚的方案是: | 取少许待测液置于试管中,滴加1~2滴FeCl3溶液.预期的实验现象和结论是 滴加FeCl3溶液后,若试管中溶液变为紫色,则丙酮中含有苯酚;若试管中溶液不变为紫色,则丙酮不含苯酚 滴加FeCl3溶液后,若试管中溶液变为紫色,则丙酮中含有苯酚;若试管中溶液不变为紫色,则丙酮不含苯酚 . |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解


| 65×(V2+V3)×10-3 |
| 22.4×m |
| 65×(V2+V3)×10-3 |
| 22.4×m |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com