
| A、蒸发氯化钠溶液时,应使混合物中的水分完全蒸干后,才能停止加热 |
| B、蒸馏石油时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C、分液操作时,下层液体从分液漏斗下口放出,上层液体从下口放出到另一个烧杯 |
| D、萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
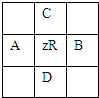 有原子序数为Z的元素R,在周期表中位于A、B、C、D四种元素中间,如图所示,
有原子序数为Z的元素R,在周期表中位于A、B、C、D四种元素中间,如图所示,| A、4Z | B、4Z+10 |
| C、4Z+5 | D、4Z+14 |
查看答案和解析>>
科目:高中化学 来源: 题型:
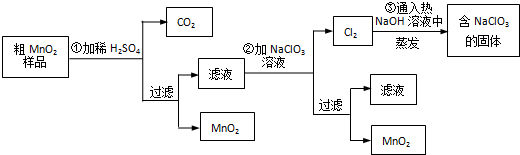
| 温 度 | 0℃ | 20℃ | 40℃ | 60℃ | 80℃ |
| NaCl 溶解度(克/100克水) | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| NaClO3溶解度(克/100克水) | 79.6 | 95.4 | 115.0 | 137.0 | 184.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C、蒸发结晶时应将溶液蒸干 |
| D、称量物质时先取小砝码,再依次取较大的砝码 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、Al3+、Cl-、CO32- |
| B、Na+、Fe2+、SO42-、NO3- |
| C、K+、Ca2+、Cl-、NO3- |
| D、K+、NH4+、OH-、SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com