
| A. | 用饱和氯化铵溶液可以清洗金属表面的锈 | |
| B. | NOx、Cl2、PM2.5颗粒都会导致酸雨 | |
| C. | 在食品袋中放入盛有硅胶的透气小袋,可防止食物受潮 | |
| D. | 人体摄入大量铝盐易患“老年性痴呆”,明矾不宜大量作净水剂 |
分析 A、饱和氯化铵溶液显酸性,铁锈中的氧化铁和酸发生反应;
B、PM2.5是造成灰霾天气的“元凶”之一,与酸雨无关,氯气不是形成酸雨的物质;
C、硅胶具有开放的多孔结构,吸附性强;
D、明矾电离出的铝离子水解生成氢氧化铝胶体,胶体具有吸附性,能净水,但铝离子摄入多,易患“老年性痴呆”.
解答 解:A、饱和氯化铵溶液中铵根离子水解显酸性,能溶解金属氧化物,所以用饱和氯化铵溶液可以清洗金属表面的锈迹,故A正确;
B、酸雨是指溶液pH小于5.6的雨水,正常雨水的pH约为5.6,二氧化硫、氮氧化物等物质是形成酸雨的重要物质,二氧化碳排放过多会引起温室效应,不是形成酸雨的气体,PM2.5是造成灰霾天气的“元凶”之一,所以Cl2、PM2.5颗粒都不会导致酸雨,故B错误;
C、硅胶具有开放的多孔结构,吸附性强,可做食品的吸水剂,可防止食物受潮,故C正确;
D、明矾的电离:KAl(SO4)2•12H2O=K++Al3++2SO42-+12H2O,电离出的Al3+水解,Al3++3H2O?Al(OH)3(胶体)+3H+,生成的氢氧化铝胶体吸附水中的悬浮物,达到净水的效果,但人体摄入大量铝盐,易患“老年性痴呆”,故D正确;
故选B.
点评 本题考查物质性质和结构的理解应用,化学与生活,化学来源于生产、生活,也服务于生产、生活,在学习过程中要理论联系实际,能运用所学知识解决实际问题,题目较简单.


 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:解答题
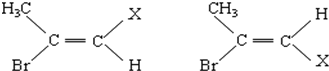
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
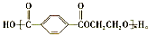 .
.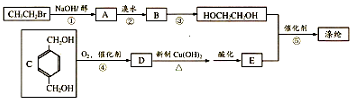
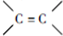 ,反应①、②的反应类型分别为消去反应、加成反应,有机物B的名称是1,2-二溴乙烷,反应③可用的试剂为氢氧化钠水溶液;
,反应①、②的反应类型分别为消去反应、加成反应,有机物B的名称是1,2-二溴乙烷,反应③可用的试剂为氢氧化钠水溶液;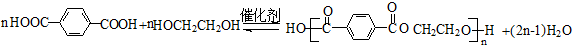 ;
;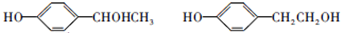 ;
;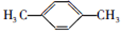 ;F的一种同系物G比F多2个碳原子,其中苯环上只有一个取代基的G的结构有4种.
;F的一种同系物G比F多2个碳原子,其中苯环上只有一个取代基的G的结构有4种.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 等物质的量浓度的Na2 C O3和NaHCO3混合液中:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) | |
| B. | 25℃时 0.2 mol•L-1盐酸与等体积0.05 mol•L-1Ba(OH)2溶液混合后,溶液的pH=l | |
| C. | pH=3的二元弱酸H2R溶液与pH=ll的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液中:2c(R2-)十c(HR-)=c(Na+) | |
| D. | 25℃时,若0.3 mol•L-1 HY溶液与0.3 mol.L-lNaOH溶液等体积混合后,溶液的 pH=9,则:c(OH-)-c(HY)-c(H+)=1×lO-9 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
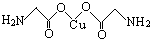
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
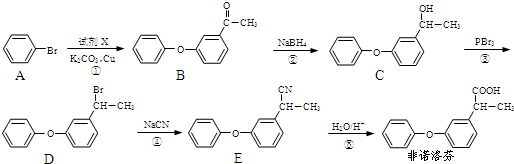
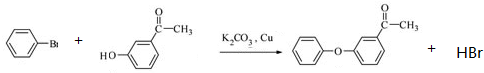 .
.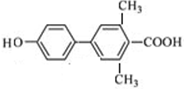 、
、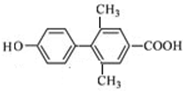 、
、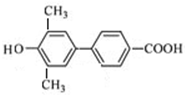 、
、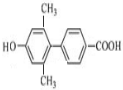 (其中一种).
(其中一种).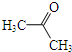 为原料制备
为原料制备 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 产物Cu2HgI4中,Cu元素的化合价为+2 | |
| B. | 由Cu2+与I-直接反应制得CuI的离子方程式为Cu2++I-=CuI | |
| C. | 该反应的氧化剂CuI,氧化产物为Cu | |
| D. | 当有2molCuI参与反应时,转移电子为1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
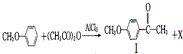
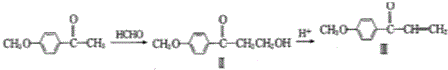
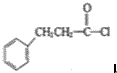 也可发生类似反应①的反应,生成化合物Ⅳ:
也可发生类似反应①的反应,生成化合物Ⅳ: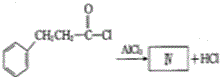
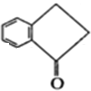 .
. .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com