
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.1 mol·L-1 Na2CO3溶液中,含CO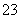 数目小于NA
数目小于NA
B.标准状况下,11.2 L O2和O3组成的混合气体含有原子数为NA
C.14 g聚乙烯与聚丙烯的混合物,含C—H键的数目为2NA
D.常温常压下,22.4 L CO2与足量Na2O2反应转移电子数为NA
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
在一定条件下,容积分别为1 L和2 L的甲、乙两密闭容器中同时充入2 mol A和2 mol B的混合气体,发生如下反应:2A(g)+B(g)xC(g) ΔH=Q kJ·mol-1,保持甲、乙两容器温度不变且相同,两容器中有关A的量随时间的变化如图:
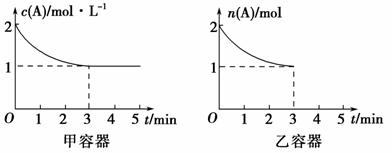
(1)根据上述图像判断,x________3(填“>”“=”或“<”)。写出该反应的平衡常数表达式:K=________,已知温度升高时,K值减小,则Q________0(填“>”“=”或“<”)。
(2)用B物质表示从0~3 min内乙容器中反应的平均速率v(B)=________。(结果保留三位小数)
(3)能说明甲容器中反应达到平衡状态的是________(填编号)。
a.2n(A)=n(B)=x·n(C)
b.c(A)、c(B)、c(C)保持一个定值
c.x·v逆(B)=v正(C)
d.甲容器中气体的密度保持不变
(4)甲、乙两容器中反应达到平衡时所耗时间相同,原因可能是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)观察如图所示的两个装置,图1装置中铜电极上产生大量的无色气泡,图2装置中铜电极上无气体产生,而铬电极上产生大量的有色气体。根据上述现象试推测金属铬具有的两种重要化学性质为
________________________________________________________________。

(2)如图是甲烷燃料电池原理示意图,回答下列问题:
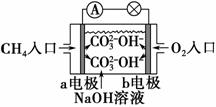
①电池的负极是________(填“a”或“b”)电极,该极的电极反应式为________________________________________________________________。
②电池工作一段时间后电解质溶液的pH________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知可逆反应温度为T0时,在容积固定的密闭容器中发生X(g)+Y(g) Z(g)(未配平)反应,各物质浓度随时间变化的关系如图a所示。其他条件相同,温度分别为T1、T2时发生反应;Z的浓度随时间变化的关系如图b所示。下列叙述正确的是( )
Z(g)(未配平)反应,各物质浓度随时间变化的关系如图a所示。其他条件相同,温度分别为T1、T2时发生反应;Z的浓度随时间变化的关系如图b所示。下列叙述正确的是( )
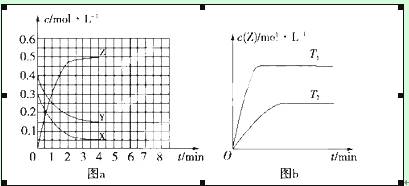
A.发生反应时,各物质的反应速率大小关系为v(X)=v(Y)=2v(Z)
B.图a中反应达到平衡时,Y的转化率为37.5%
C.T0时,该反应的平衡常数为33.3 D.该反应正反应的反应热ΔH<0
查看答案和解析>>
科目:高中化学 来源: 题型:
能源、环境与人类生活和社会发展密切相关,研究它们的综合利用有重要意义。
(1)氧化—还原法消除氮氧化物的转化如下: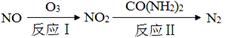
①反应Ⅰ为:NO+O3=NO2+O2,生成11.2 L O2(标准状况)时,转移电子的物质的量是 mol。
②反应Ⅱ中,当n(NO2)∶n[CO(NH2)2]=3∶2时,反应的化学方程式是 。
(2)硝化法是一种古老的生产硫酸的方法,同时实现了氮氧化物的循环转化,主要反应为:NO2(g)+SO2(g)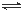 SO3(g)+NO(g) △H=-41.8 kJ·mol-1已知:2SO2(g)+O2(g)
SO3(g)+NO(g) △H=-41.8 kJ·mol-1已知:2SO2(g)+O2(g)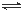 2SO3(g) △H=-196.6 kJ·mol-1,写出NO和O2反应生成NO2的热化学方程式 。
2SO3(g) △H=-196.6 kJ·mol-1,写出NO和O2反应生成NO2的热化学方程式 。
某化学兴趣小组构想将NO转化为HNO3,装置如下图一,电极为多孔惰性材料。则负极的电极反应式是 。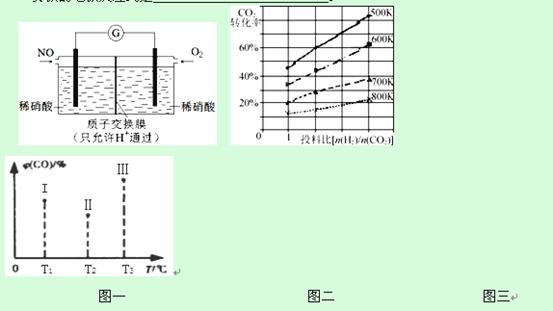
(4)将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g);
CH3OCH3(g)+3H2O(g);
①该反应平衡常数表达式为K= 。
②已知在某压强下,该反应在不同温度、不同投料比时,CO2的转化率如右图二所示。该反应的ΔH________(填“>”、“<”或“=”)0。
(5)合成气CO和H2在一定条件下能发生如下反应:CO(g) +2H2(g) CH3OH(g) △H<0。在容积均为VL的I、Ⅱ、Ⅲ三个相同密闭容器中分别充入amol CO和2a mol H2,三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下,实验测得反应均进行到t min时CO的体积分数如图三所示,此时I、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是 ;若三个容器内的反应都达到化学平衡时,CO转化率最大的反应温度是 。
CH3OH(g) △H<0。在容积均为VL的I、Ⅱ、Ⅲ三个相同密闭容器中分别充入amol CO和2a mol H2,三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下,实验测得反应均进行到t min时CO的体积分数如图三所示,此时I、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是 ;若三个容器内的反应都达到化学平衡时,CO转化率最大的反应温度是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.常温下,0.05 mol·L-1 Fe2(SO4)3溶液中含Fe3+数目为0.1NA
B.标准状况下,22.4 L甲苯中含C—H数目为8NA
C.常温常压下,3.2 g O2和O3混合物中,氧原子的数目为0.2NA
D.0.1 mol Na2O2与足量CO2反应时,转移的电子数目为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
1 000 K时反应C(s)+2H2(g)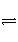
 CH4(g)的K=8.28×107 (mol·L-1)-1,当各气体物质的量浓度分别为H2 0.7 mol·L-1、CH4 0.2 mol·L-1时,上述反应( )
CH4(g)的K=8.28×107 (mol·L-1)-1,当各气体物质的量浓度分别为H2 0.7 mol·L-1、CH4 0.2 mol·L-1时,上述反应( )
A.正向移动 B.逆向移动 C.达到平衡 D.不一定
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于聚乙炔的叙述中错误的是( )
A.聚乙炔是高分子化合物
B.聚乙炔是加聚反应的产物
C.聚乙炔在空气中很稳定、难溶解
D.聚乙炔的结构简式是CH===CH
查看答案和解析>>
科目:高中化学 来源: 题型:
下图表示有关的一种反应物或生成物(无关物质已略去),其中A、C为无色气体,请填写下列空白。
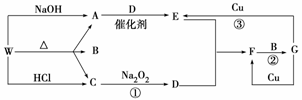
(1)化合物W可能是____________或__________,C是____________,F是____________。
(2)反应①中若消耗Na2O2 7.8 g,则转移的电子数为_________________________。
(3)反应③的离子方程式:________________________________________________。
(4)A与CuO在加热条件下能反应生成N2和Cu,请写出该反应的化学方程式:
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com