
| A、金属镁的熔点高于金属铝 |
| B、碱金属单质的熔、沸点从Li到Cs是逐渐升高的 |
| C、金属镁的硬度小于金属钙 |
| D、金属铝的硬度大于金属钠 |


科目:高中化学 来源: 题型:
| ||

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、奥运会火炬的燃料丙烷是有机物 |
| B、用少量食醋除去水壶中的水垢 |
| C、日常生活中无水乙醇常用于杀菌消毒 |
| D、浓硝酸溅到皮肤上,使皮肤变黄色,是由于浓硝酸和蛋白质发生颜色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
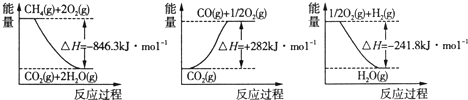
| ||
| △ |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、是发达国家对贫穷国家的一种援助形式 |
| B、是发达国家企业逃避高额处理费用,转移垃圾的行为 |
| C、带动了本地经济和就业,促进了经济的可持续发展 |
| D、进口国少数人获利,广大工人的健康和国家上台环境受到严重破坏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向溶液X中加入稀盐酸,并将产生的无色气体通入澄清石灰水中 | 生成白色沉淀 | 溶液X中一定含有CO32-或HCO3- |
| B | 向某溶液中先滴加盐酸无现象,再滴加BaCl2溶液 | 有白色沉淀生成 | 原溶液中含有SO42- |
| C | 分别测定同温 同浓度NaCl与CH3COONa溶液的pH | CH3COONa溶液的pH小 | 盐酸的酸性强于醋酸的酸性 |
| D | 向无水乙醇中加入浓H2SO4,加热至170℃将产生的气体通入酸性KMnO4 溶液 | 紫红色褪去 | 使溶液褪色的不一定是乙烯 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、实验室用氯酸钾受热分解制取氧气 |
| B、实验室用过氧化氢的水溶液分解制取氧气 |
| C、实验室用碳酸钙制取二氧化碳 |
| D、实验室用电石和水制取乙炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、8种 | B、16种 |
| C、32种 | D、40种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、先加入酸性高锰酸钾溶液;后加银氨溶液,水浴加热 |
| B、先加入溴水;后加酸性高锰酸钾溶液 |
| C、先加入新制氢氧化铜悬浊液,加热;再加入溴水 |
| D、先加入银氨溶液;再另取该物质加入溴水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com