
【题目】锌与不同浓度的硫酸反应时,硫酸的还原产物为SO2或H2。为验证这一事实,某同学用下图装置在室温下进行实验。
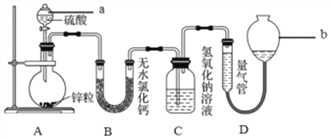
请回答下列问题:
(1)仪器a的名称是_________,若在圆底烧瓶中放入1.0g锌,选用量气管的适宜规格是(按标况计算)_____ (填字母序号)。
A.200mL B.300mL C.400mL D.500mL
(2)按上图连接好装置后,检查A装置气密性的操作是____,为使仪器a中的硫酸顺利加入圆底烧瓶,应_____并旋转活塞。
(3)实验发现:1.0g锌完全溶解后氢氧化钠洗气瓶增重0.8g,写出圆底烧瓶中发生反应的化学方程式:_________________。
(4)若ag锌与cmol/L的硫酸VL充分反应后锌有剩余,测得氢氧化钠洗气瓶增重mg,则整个实验过程产生的气体中, ![]() =______(用含字母的代数式表示), 若撤走B装置,
=______(用含字母的代数式表示), 若撤走B装置, ![]() 的数值将______(填“偏大”、“偏小”或“无影响”),其原因是________________。
的数值将______(填“偏大”、“偏小”或“无影响”),其原因是________________。
(5)为准确测量气体体积,量气管在读数时应注意的操作有_______。
【答案】 分液漏斗 C 关闭分液漏斗(或 a) 活塞,用热毛巾(或双手) 捂热圆底烧瓶, 一段时间后 C中浸入液体中的导气管末端有气泡冒出, 移开热毛巾(或双手)后 C 中导气管中上升一段稳定的水柱(其它合理答案也可) 打开分液漏斗(或 a)的瓶塞(或玻璃塞)(或使瓶塞上的凹槽对准分液漏斗颈部的小孔) Zn + 2H2SO4(浓) ===ZnSO4 + SO2↑+ H2O 、Zn + H2SO4 === ZnSO4 + H2↑ ![]() 偏小 A 中产生的水蒸气进入装置 C 中使得计算的 n(SO2)偏大 读数前移动 b 使量气管左右液面相平; ②视线与量气管凹液面最低点在同一水平面 ③待装置冷却至室温读数
偏小 A 中产生的水蒸气进入装置 C 中使得计算的 n(SO2)偏大 读数前移动 b 使量气管左右液面相平; ②视线与量气管凹液面最低点在同一水平面 ③待装置冷却至室温读数
【解析】(1)由装置图可得,仪器a是分液漏斗;C中盛有氢氧化钠溶液,则量气管D测量的是氢气的体积,根据反应Zn+H2SO4=ZnSO4+H2↑,n(H2)=n(Zn)=1.0g÷65g/mol=![]() mol,则标准状况下V(H2)=
mol,则标准状况下V(H2)= ![]() mol×22.4L/mol=
mol×22.4L/mol=![]() L≈344.6mL,所以选用量气管的适宜规格是400mL,故选C。
L≈344.6mL,所以选用量气管的适宜规格是400mL,故选C。
(2)检查装置气密性,首先要密闭,应关闭分液漏斗(a)活塞,然后形成压强差,并产生明显现象,应微热圆底烧瓶,所以检查A装置气密性的操作可以是:关闭分液漏斗(a)活塞,用热毛巾(或双手)捂热圆底烧瓶,一段时间后C中浸入液体中的导气管末端有气泡冒出,移开热毛巾(或双手)后C中导气管中上升一段稳定的水柱,则气密性良好。为使仪器a(分液漏斗)中的硫酸顺利加入圆底烧瓶,需要平衡a(分液漏斗)中压强,使之与空气连通,故应打开分液漏斗(a)的瓶塞(玻璃塞)(或者使瓶塞上的凹槽对准分液漏斗颈部的小孔)。
(3)氢氧化钠吸收的是SO2气体,所以一定发生反应:Zn+2H2SO4(浓)=ZnSO4+SO2↑+H2O,0.8gSO2的物质的量为:0.8g÷64g/mol=0.0125mol,1.0g锌的物质的量为:1.0g÷65g/mol≈0.0154mol>0.0125mol,所以还会发生反应:Zn+H2SO4=ZnSO4+H2↑。
(4)由已知,n(H2SO4)=cVmol,氢氧化钠洗气瓶增重mg,则n(SO2)= ![]() mol,根据反应Zn+2H2SO4(浓)=ZnSO4+SO2↑+H2O,消耗硫酸为2×
mol,根据反应Zn+2H2SO4(浓)=ZnSO4+SO2↑+H2O,消耗硫酸为2×![]() mol,所以生成H2的H2SO4为:(cV-2×
mol,所以生成H2的H2SO4为:(cV-2×![]() )mol,则n(H2)=(cV-2×
)mol,则n(H2)=(cV-2×![]() )mol,故
)mol,故![]() =
=![]() 。若撤走B装置,A中产生的水蒸气进入装置C中使n(SO2)的计算结果偏大,则算得n(H2)偏小,
。若撤走B装置,A中产生的水蒸气进入装置C中使n(SO2)的计算结果偏大,则算得n(H2)偏小, ![]() 的数值将偏小。
的数值将偏小。
(5)Zn与硫酸的反应是放热反应,温度升高,气体受热膨胀,此时读出的气体体积偏大,因此要恢复到室温状态;因为测得的体积需要转化到标准状况,而量气管中的压强不容易测量,可以调节量气管左右液面相平,量气管中的压强即等于室内压强;读数时,视线与凹液面最低处相平,总之为准确测量气体体积,量气管在读数时要消除内外气体压强不相等及视线不正确而造成的误差,所以应注意的操作有:①读数前移动b使量气管左右液面相平;②视线与量气管凹液面最低点在同一水平面;③待装置冷却至室温读数。


科目:高中化学 来源: 题型:
【题目】已知:①H+(aq)+OH﹣(aq)═H2O(l);△H1;②2SO2(g)+O2(g)2SO3(g);△H2 . 其他条件不变时,改变反应物的量,则下列判断正确的是( )
A.△H1 , △H2都不变
B.△H1 , △H2都增大
C.△H1 , △H2都减小
D.不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某潜艇上的核反应堆内使用了液体铝钠合金作载热介质,下列关于Al、Na原子结构的分析中正确的是
A. 原子半径:Al>Na B. 第一电离能:Al<Na
C. 基态原子未成对电子数:Na = Al D. 硬度:Na>Al
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将m g含氧化铁、氧化铜或氧化亚铁的样品投入物质的量浓度为1 mol/L的2 L盐酸中恰好完全反应,若向等质量的该样品中通入足量的氢气并加热,充分反应后所得金属的质量是 ( )
A. (m-16)g B. (m+16)g
C. (m-32)g D. 16g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G 七种烃的分子球棍模型如图所示,据此回答下列问题:
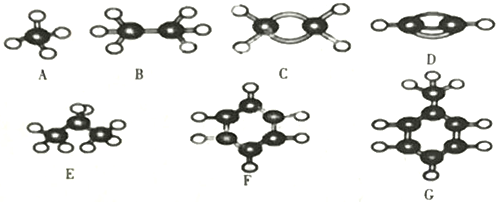
(1)能够发生加成反应的烃有_____________种。
(2)与A互为同系物的是__________(填字母)。
(3)工业上可用有机物C来合成乙醇,写出该反应的化学方程式:__________________________。
(4)烯烃在一定条件下被氧化时,由于![]() 断裂,转化为醛或酮。如:
断裂,转化为醛或酮。如:
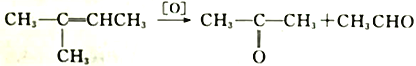
某有机物H与上述有机物C互为同系物,其所含碳原子数是有机物C的4倍,发生上述类似条件的反应时只有一种产物,且该产物不能发生银镜反应,写出该产物的结构简式: _______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硫化铜精矿为原料生产CuCl的工艺过程如下:
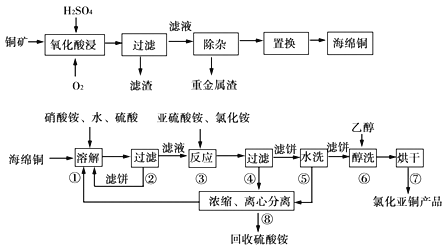
已知CuCl难溶于醇和水,可溶于氯离子浓度较大的伓系,在潮湿空气中易水解氧化,海绵铜Cu中含少量CuO等。
(1)经测定氧化酸浸过程有单质S生成,写出此过程中的化学方程式_____________
(2)步骤①中得到的氧化产物是____________,溶解温度应控制在60—70℃,原因是_____________。
(3)写出步骤③中主要反应的离子方程式_____________。
(4)步骤③先加NH4Cl、再加入亚硫酸铵时无沉淀,加水稀释就产生大量臼色沉淀,其原因_____________。
(5)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是_____________(写名称)。
(6)上述工艺中,步骤⑥不能省略,理由是_____________。
(7)上述浓缩液中含有Iˉ、CIˉ等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中中![]() 为_____________。(已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17)
为_____________。(已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17)
(8)准确称取所制备的氯化亚铜样品m g,将其置于过量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用a mol·L-1的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7,溶液b mL,反应中Cr2O72-被还原为Cr3+,样品中CuCl的质量分数为_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列文字表述与反应的离子方程式对应且正确的是 ( )
A. 溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+=AgBr↓
B. 用醋酸除去水垢:CaCO3 + 2H+=Ca2+ + H2O + CO2↑
C. 苯酚与纯碱溶液混合:2C6H5OH + CO32- ![]() CO2 ↑+ H2O + 2C6H5O-
CO2 ↑+ H2O + 2C6H5O-
D. 甲醛溶液与足量的银氨溶液共热:HCHO+4Ag(NH3)2++4OH-![]() CO32-+2NH4++4Ag↓+6NH3+2H2O
CO32-+2NH4++4Ag↓+6NH3+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z、N、M六种主族元素,它们在周期表中位置如图所示,下列说法不正确的是
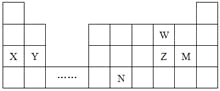
A. 原子半径:Y>Z>W
B. 单质的还原性:X>Y
C. 溴与元素M同主族,最高价氧化物的水化物的酸性比M的强
D. 元素N位于金属与非金属的分界线附近,可以推断N元素的单质可作半导体材料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com