
【题目】如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是:( )
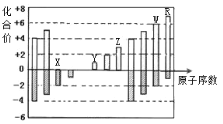
A. 原子半径:Z>Y>X
B. 气态氢化物的稳定性:R>W
C. WX3和水反应形成的化合物是离子化合物
D. Y和Z两者最高价氧化物对应的水化物的碱性:Z>Y
【答案】B
【解析】
由表中化合价可知,X的化合价为-2价,没有正化合价,故X为O元素,Y的化合价为+1价,处于ⅠA族,原子序数大于O元素,故Y为Na元素,Z为+3价,为Al元素,W的化合价为+6、-2价,故W为S元素,R的最高正价为+7价,应为Cl元素,所以X为O,Y为Na,Z为Al,W为S,R为Cl;
A.已知X为O,Y为Na,Z为Al,原子半径应为Na>Al>O,故A错误;
B.已知W为S,R为Cl,非金属性Cl>S,则气态氢化物的稳定性Cl>S,故B正确;
C.X为O,W为S,所以WX3和水反应形成的化合物是硫酸,是共价化合物,故C错误;
D.Z为Al,Y为Na,金属性Na>Al,金属性越强,最高价氧化物对应的水化物碱性越强,则两者最高价氧化物对应的水化物碱性NaOH>Al(OH)3,故D错误;
故选:B。


科目:高中化学 来源: 题型:
【题目】某有机物A的结构简式为  ,取Na、NaOH、NaHCO3分别与等物质的量的该物质恰好反应(反应时可加热煮沸),则Na、NaOH、NaHCO3三种物质的物质的量为
,取Na、NaOH、NaHCO3分别与等物质的量的该物质恰好反应(反应时可加热煮沸),则Na、NaOH、NaHCO3三种物质的物质的量为
A. 2:2 :1 B. 1:1:1 C. 3:2:1 D. 3:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:常温下,气体A为无色有毒气体,气体B为黄绿色气体,请根据下图完成填空。

(1)A是________,E是________;
(2)A与B在水溶液中反应的离子方程式是:______;
(3)分别将气体A与B通入如下装置,待一段时间后,分别加热甲、乙两支试管。
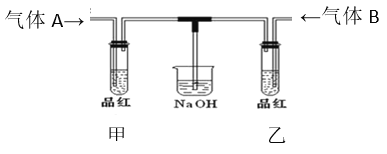
①试管甲中的实验现象为_______________,原因是_________________________;
②试管乙中的实验现象为_________________________,原因是___________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 化石燃料不一定在任何条件下都能充分燃烧
B. 化石燃料在燃烧过程中能产生污染环境的CO、SO2等有害气体
C. 直接燃烧煤不如将煤进行深加工后再燃烧的效果好
D. 固体煤变为气体燃料后,燃烧效率将更低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1.013×105 Pa下,测得的某些烷烃的沸点见下表。据表分析,下列说法正确的是( )
物质名称 | 沸点/℃ |
正丁烷CH3(CH2)2CH3 | -0.5 |
正戊烷CH3(CH2)3CH3 | 36.1 |
异戊烷 | 27.8 |
新戊烷 | 9.5 |
正己烷CH3(CH2)4CH3 | 69.0 |
A. 在标准状况时,新戊烷是气体
B. 在1.013×105 Pa、20 ℃时,C5H12都是液体
C. 烷烃随碳原子数增加,沸点降低
D. C5H12随支链增加,沸点降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图甲中①②③④表示不同化学元素所组成的化合物,图乙表示由四个单体构成的化合物。以下说法不正确的是( )
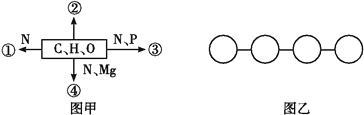
A. 若图甲中的②大量存在于皮下和内脏器官周围等部位,则②是脂肪
B. 若图甲中④能吸收、传递和转换光能,则④可用无水乙醇提取
C. 图乙中若单体是氨基酸,则该化合物彻底水解后的产物中氧原子数增加3个
D. 图乙中若单体是四种脱氧核苷酸,则该化合物彻底水解后的产物有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是
A. 1L 0.1mol·L-1NaHSO3溶液中含有H+的数目为NA个
B. 常温常压下,等质量的CO2和N2O的气体体积相等
C. 60g组成为C2H4O2的有机物含C-H键数目一定为3NA个
D. 25℃时,pH=1的H3PO4溶液中含有的H+数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼酸钠晶体(Na2MoO4·2H2O)常用于制造阻燃剂和无公害型冷水系统的金属抑制剂。下图是利用钼精矿(主要成分是MoS2,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图:

回答下列问题:
(1)提高焙烧效率的方法有____________。(写一种)
(2)“焙烧”时MoS2转化为MoO3,该反应过程的化学方程式为________________________,氧化产物是________(写化学式)。
(3)“碱浸”时含钼化合物发生的主要反应的化学方程式为__________________________。
(4)若“除重金属离子”时加入的沉淀剂为Na2S,则废渣成分的化学式为________。
(5)测得“除重金属离子”中部分离子的浓度:c(MoO42-)=0.40mol/L,c(SO42-)=0.04mol/L。“结晶”前需先除去SO42-,方法是加入Ba(OH)2固体。假设加入Ba(OH)2固体后溶液体积不变,当SO42-完全沉淀(c(SO42-)≤1.0×10-5mol/L)时,BaMoO4是否会析出?____________________________________。(请计算说明)[已知:Ksp(BaSO4)=1.1×10-10,Ksp(BaMoO4)=4.0×10-8]
(6)钼精矿在碱性条件下,加入NaClO溶液,也可以制备钼酸钠,同时有SO42-生成,该反应的离子方程式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种常见的单质,B、C为常见的化合物,A、B、C均含有元素x,它们有如图所示的转化关系(部分产物及反应条件已略去)。下列说法中正确的是( )
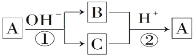
A. 反应①和②一定为氧化还原反应
B. 反应①和②互为可逆反应
C. X元素可能是金属,也可能是非金属
D. X元素可能为铝
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com