
分析 (1)铁粉足量,盐酸中氢离子完全生成氢气,根据氢离子的物质的量计算出生成氢气的物质的量,再根据V=nVm计算出生成氢气的体积;
(2)混合后溶液中c(Cl-)=c(HCl)+2c(CuCl2),反应后的溶液全部是FeCl2溶液,c(Fe2+)=c(FeCl2)=$\frac{1}{2}$c(Cl-).
解答 解:(1)2L 1.0mol/LHCl 溶液中含有HCl的物质的量为:1.0mol/L×2L=2mol,则混合液中含有2mol氢离子,由于铁粉过量,则2mol氢离子完全反应生成氢气的物质的量为:2mol×$\frac{1}{2}$=1mol,标准状况下1mol氢气的体积为:22.4L/mol×1mol=22.4L,
答:混合后生成标准状况下氢气的体积为22.4L;
(2)把2.0mol/LCuCl2溶液和1.0mol/LHCl溶液各取2L混合(假设混合后溶液总体积为4L),混合液中氯离子的总浓度为:c(Cl-)=$\frac{2.0mol/L×2×2L+1.0mol/L×2L}{4L}$=2.5mol/L,
混合液中加入足量铁粉,反应后的溶液中的溶质为FeCl2,则c(Fe2+)=c(FeCl2)=$\frac{1}{2}$c(Cl-)=2.5mol/L×$\frac{1}{2}$=1.25mol/L,
答:反应后溶液中Fe2+的物质的量浓度为1.25mol/L.
点评 本题考查物质的量浓度有关计算,题目难度中等,注意稀释定律的运用,注意对公式的理解与灵活运用,理解电解质浓度与电解质离子浓度关系,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:选择题
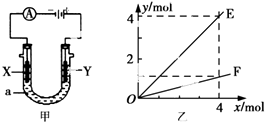
| A. | 若此装置用于电解精炼铜,则X为纯铜、Y为粗铜,电解的溶液a可以是硫酸铜或氯化铜溶液 | |
| B. | 按图甲装置用惰性电极电解AgNO3溶液,若图乙横坐标x表示流入电极的电子的物质的量,则E可表示反应生成硝酸的物质的量,F表示电解生成气体的物质的量 | |
| C. | 按图甲装置用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,加入0.5 mol的碳酸铜刚好恢复到通电前的浓度和pH,则电解过程中转移的电子为2.0 mol | |
| D. | 若X、Y为铂电极,a溶液为500 mL KCl和KNO3的混合液,经过一段时间后,两极均得到标准状况下11.2 L气体,则原混合液中KCl的物质的量浓度至少为2.0 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化剂和还原剂的物质的量之比为1:8 | |
| B. | 当有1mol Cl2生成时,有0.5 mol电子发生转移 | |
| C. | 氧化产物是MnCl2,还原产物Cl2 | |
| D. | 相同物质的量的KMnO4和MnO2分别与足量浓盐酸充分反应产生Cl2质量之比为5:2. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2 | B. | 2:3 | C. | 3:2 | D. | 1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 46gNO2和N2O4混合气体中含有原子总数为3NA | |
| B. | 1molCl2与足量的铁反应,转移的电子数为2NA | |
| C. | 常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.2NA | |
| D. | 1 mol Na 与足量O2 反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | KClO3在反应中得到电子 | |
| B. | ClO2是还原产物 | |
| C. | H2C2O4在反应中被还原 | |
| D. | 1mol H2C2O4参加反应有2mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有②③ | B. | 只有③④ | C. | 都正确 | D. | 都错误 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a c f h | B. | a c e g | C. | a c e f h | D. | b d e h |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 与乙苯互为同系物 | B. | 分子中共直线的原子最多有4个 | ||
| C. | 分子中共平面的碳原子最多有13个 | D. | 与甲苯互为同分异构体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com