
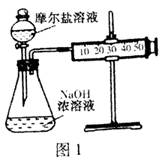
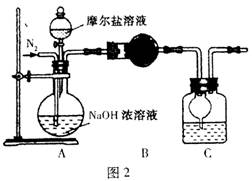


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
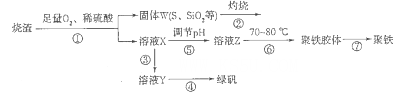
 2K2S+K2SO3+3H2O,该反应的氧化剂与还原剂质量之比为___________。
2K2S+K2SO3+3H2O,该反应的氧化剂与还原剂质量之比为___________。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
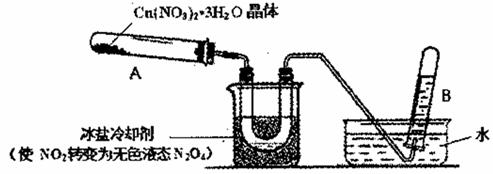
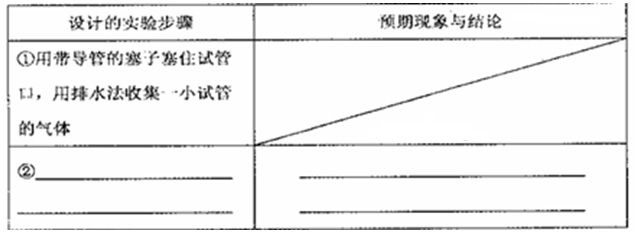
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 6SO2+Fe3O4,有3 mol FeS2参加反应,转移________ mol电子。
6SO2+Fe3O4,有3 mol FeS2参加反应,转移________ mol电子。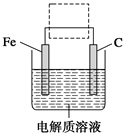
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将铜粉和硫粉混合均匀并加热以制取CuS |
| B.将Cu片放入过量浓硫酸中,一段时间后加水以观察CuSO4溶液的颜色 |
| C.向CuSO4溶液中加入NaOH溶液,过滤洗涤并收集沉淀,加热以制取CuO |
| D.设计Cu—Al—浓硝酸原电池,以证明金属活动性:Cu<Al |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验步骤 | 预期现象与结论 |
| 步骤1:取2mLFeSO4溶液和2mLKI溶液混合于试管中,再滴加1~2滴氯水。 | ; |
| 步骤2:____________________________________ ____________________________________。 | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 样品含有少量
样品含有少量 杂质。现要测定其中
杂质。现要测定其中 的质量分数,实验按以下步骤进行:
的质量分数,实验按以下步骤进行:

 溶液18.00mL。该样品中
溶液18.00mL。该样品中 (式量为270.5)的质量分数为_____________。
(式量为270.5)的质量分数为_____________。 杂质除去,可用的试剂是________(选填编号)。
杂质除去,可用的试剂是________(选填编号)。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com