
分析 先根据n=$\frac{N}{{N}_{A}}$计算出1.204×1023个H218O的物质的量,然后根据m=nM计算出其质量;标准状况下气体摩尔体积为22.4L/mol,根据V=nVm=$\frac{m}{M}$Vm计算出标准状况下二氧化氮的体积.
解答 解:1.204×1023个H218O的物质的量为:$\frac{1.204×1{0}^{23}}{6.02×1{0}^{23}mo{l}^{-1}}$=0.2mol,其质量为:20g/mol×0.2mol=4.0g;
11.5gNO2的物质的量为:$\frac{11.5g}{46g/mol}$=0.25mol,标准状况下0.25mol二氧化氮的体积为:22.4L/mol×0.25mol=5.6L,
故答案为:4.0;5.6.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔质量、气体摩尔体积、阿伏伽德罗常数之间的关系为解答关键,试题侧重基础知识的考查,培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:解答题
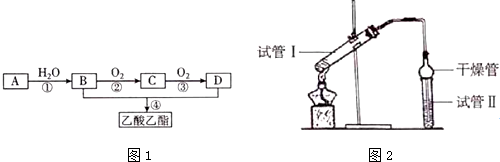
| 实验编号 | 试管I中试剂 | 试管Ⅱ中有机层的厚度/cm |
| A | 3mL乙醇、2mL乙酸、2mL 18mol•L-1浓硫酸 | 3.0 |
| B | 3mL乙醇、2mL乙酸 | 0.1 |
| C | 3mL 乙醇、2mL 乙酸 2mL3mol•L-1H2SO4 | 0.6 |
| D | 3mL乙醇、2mL乙酸、盐酸 | 0.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 每生成0.3molH2,被还原的水分子数目为0.6NA | |
| B. | 当有2.7gAl参加反应时,转移的电子数目为0.3NA | |
| C. | 每生成6.72L的H2,溶液中AlO2-的数目就增加0.2NA | |
| D. | 溶液中每增加0.1mol的AlO2-,Na+的数目就增加0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
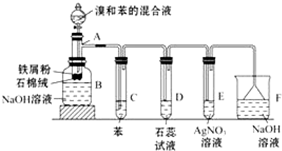 图为苯和溴的取代反应的实验装置图,其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑粉.
图为苯和溴的取代反应的实验装置图,其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑粉. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaCO3高温?CaO+CO2↑ | |
| B. | Pb+PbO2+2H2SO4?充电放电2PbSO4+2H2O | |
| C. | 2H2O 电解?2H2↑+O2↑ | |
| D. | 6nH2O+6nCO2→叶绿体光(C6H12O6)n+6nH2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 自然界里Na元素只以化合态存在 | |
| B. | 钠与水反应放出氧气 | |
| C. | 钠放置在空气中很快被氧化为白色Na2O2 | |
| D. | 钠投入稀CuSO4溶液中,可置换出金属Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com