
在日常生活中,与化学反应速度有关的做法是( )
|
| A. | 用热水溶解蔗糖以加速溶解 |
|
| B. | 把块状煤碾成粉末状再燃烧 |
|
| C. | 真空包装食品,以延长保质期 |
|
| D. | 低温冷藏使食品延缓变质 |
考点:
化学反应速率的影响因素.
专题:
化学反应速率专题.
分析:
A、温度升高加速蔗糖分子的运动,但蔗糖溶解属于物理变化;
B、把块状煤碾成粉末状,增大与氧气的接触面积;
C、真空包装隔绝氧气,抑制微生物的繁殖,延缓食品变质;
D、采用冷藏的方法储存食品时,温度低,微粒的运动速率慢,食品缓慢氧化的速率慢,保质期就长.
解答:
解:A、温度升高加速蔗糖分子的运动,使蔗糖溶解加速,但蔗糖溶解属于物理变化,不是化学变化,故A错误;
B、把块状煤碾成粉末状,增大与氧气的接触面积,加快煤的燃烧,故B正确;
C、真空包装隔绝氧气,抑制微生物的繁殖,延缓食品变质,保质期长,故C正确;
D、采用冷藏的方法储存食品时,温度低,微粒的运动速率慢,食品缓慢氧化的速率慢,保质期就长,故D正确;
故选BCD.
点评:
考查反应速率的影响因素等,难度不大,注意基础知识的掌握与理解.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
实验室用如图所示装置制备干燥纯净的氯气,并进行氯气的性质实验.请回答下列问题:
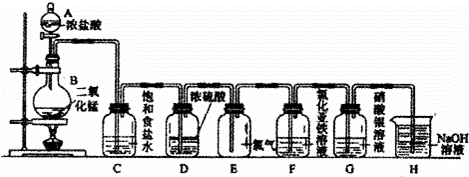
(1)A中盛有浓盐酸,B中盛有MnO2,则烧瓶中发生反应的离子方程式为:;
(2)C中盛有饱和食盐水,其作用是,D中浓硫酸的作用是.
(3)F中是FeCl2溶液,F中发生反应的离子方程式为;
(4)G中是AgNO溶液,现象是
(5)H中盛有Na0H溶液,其作用是.
(6)若用200mL10mol•L﹣1的浓盐酸与足量的二氧化锰固体加热反应(不考虑氯化氢挥发),则产生氯气的物质的量为0.5mol(填“大于”、“等于”或“小于”),若用8.7g二氧化锰与足量的浓盐酸反应,则被氧化的氯化氢的物质的量是.
查看答案和解析>>
科目:高中化学 来源: 题型:
下面食谱营养搭配最均衡的是( )
|
| A. | 凉拌青菜、土豆丝、馒头 |
|
| B. | 糖醋排骨、清蒸鲈鱼、米饭 |
|
| C. | 虾仁白菜、红烧带鱼、酸菜炖猪蹄、萝卜汤 |
|
| D. | 酱牛肉、炒油菜、红烧豆腐、西红柿蛋汤、馒头 |
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃,水的电离达到平衡:H2O⇌H++OH﹣,下列叙述正确的是( )
|
| A. | 向水中加入稀醋酸,平衡逆向移动,c(H+)降低 |
|
| B. | 向水中加入少量固体碳酸氢钠,c(H+)增大,Kw不变 |
|
| C. | 向水中加入少量固体CH3COONa,平衡正向移动,c(H+)降低 |
|
| D. | 将水加热,Kw增大,pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在BaSO3(s)⇌Ba2+(aq)+SO32﹣ (aq)平衡体系中,下列措施可使沉淀量减少的是( )
|
| A. | 加入K2SO3(s) | B. | 加入稀HNO3 | C. | 加入稀盐酸 | D. | 加入K2SO4(s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42﹣、CO32﹣等离子.当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图象如图所示,下列说法正确的是()
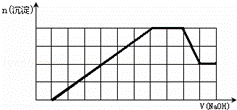
A. 原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+
B. 原溶液中一定含有SO42﹣和Na+
C. 原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
D. 反应最后形成的溶液中含有的溶质为Na2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com