
| 放电 |
| 充电 |
| A、构成该电池的正极和负极必须是两种活性不同的金属 |
| B、充电时有CH3OH生成的电极为阳极 |
| C、放电时溶液中的OH-移向正极 |
| D、放电时负极的电极反应为:CH3OH-6e-+8OH-═CO32-+6H2O |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
 已知A、B、C、D、E、F六种短周期元素中,A、B、C、D是组成蛋白质的基本元素;A与B的原子序数之和等于C原子核内的质子数;A与E、D与F分别位于同一主族,E与F同周期,且F原子核内的质子数是D原子核外电子数的2倍.据此请回答:
已知A、B、C、D、E、F六种短周期元素中,A、B、C、D是组成蛋白质的基本元素;A与B的原子序数之和等于C原子核内的质子数;A与E、D与F分别位于同一主族,E与F同周期,且F原子核内的质子数是D原子核外电子数的2倍.据此请回答:查看答案和解析>>
科目:高中化学 来源: 题型:

| A、当两电池转移相同电子时,生成和消耗Ni的物质的量相同 |
| B、两装置工作时,盐桥中的阴离子向负极移动,阳离子向正极移动 |
| C、由此可判断能够发生2Cr3++3Ni=3Ni2++2Cr和Ni2++Sn=Sn2++Ni的反应 |
| D、由此可判断Cr、Ni、Sn三种金属的还原性强弱顺序为:Cr>Ni>Sn |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol/L的NaOH溶液中Na+的物质的量为1mol |
| B、28g乙烯所含共用电子对数目为4NA |
| C、常温常压下,32g O2与O3的混合气体中含有的原子总数为2NA |
| D、1mol苯中含有碳碳双键的数目为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X是钠元素 |
| B、离子半径X+>Z2- |
| C、同族元素中Z的氢化物稳定性最强 |
| D、同周期元素中Y的非金属性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用碳酸钠溶液处理水垢中的硫酸钙:Ca2++CO32-=CaCO3↓ | ||||
| B、SO2使紫色石蕊溶液变红色:SO2+H2O=2H++SO32- | ||||
| C、用石墨电极电解AlCl3溶液,阴极附近生成沉淀:2Al3++6H2O+6e-=2Al(OH)3↓+3H2↑ | ||||
D、工业上制取硅:SiO2+C
|
查看答案和解析>>
科目:高中化学 来源: 题型:
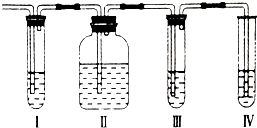 在实验室里制取的乙烯中常混有少量的二氧化硫,某化学兴趣小组设计了如图所示的实验装置以确认上述混合气体中是否含有SO2和C2H4.请回答下列问题:
在实验室里制取的乙烯中常混有少量的二氧化硫,某化学兴趣小组设计了如图所示的实验装置以确认上述混合气体中是否含有SO2和C2H4.请回答下列问题:| 光照 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com