
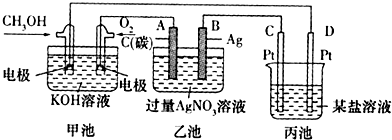
分析 甲中负极为甲醇,正极为氧气,为原电池,负极反应为CH3OH+8OH-6e-═CO32-+6H2O,乙为电解池,A与原电池的正极相连,则A为阳极,发生4AgNO3+2H2O$\frac{\underline{\;电解\;}}{\;}$4Ag+O2↑+4HNO3,乙中B极析出Ag,阴极生成氧气,利用电子守恒可知,O2~4Ag~4HNO3,丙池某电极析出1.60g某金属,氧化性比氢离子强的金属离子均可能,以此来解答.
解答 解:(1)由图可知,甲为燃料电池,则为原电池,甲为乙的电源,则乙为电解池,丙池是也是电解池,阳离子向正极移动,氧气是正极,故答案为:电解池;O2;(2)通CH3OH的电极为负极,发生氧化反应,电解反应式为:CH3OH-6e-+8OH-=CO32-+6H2O,故答案为:CH3OH-6e-+8OH-=CO32-+6H2O;
(3)乙池中阳极氢氧根离子放电,生成氧气,产生氢离子,溶液呈酸性,所以A极附近变红,故答案为:A;
(4)乙为电解池,A与原电池的正极相连,则A为阳极,溶液中银离子、氢氧根离子放电,发生4AgNO3+2H2O$\frac{\underline{\;通电\;}}{\;}$4Ag+O2↑+4HNO3,乙池中总反应的离子方程式4Ag++2H2O$\frac{\underline{\;通电\;}}{\;}$4Ag+O2↑+4H+,故答案为:4Ag++2H2O$\frac{\underline{\;通电\;}}{\;}$4Ag+O2↑+4H+;
(5)由电子守恒可知,O2~4Ag~4HNO3,n(O2)=$\frac{5.4g}{108g/mol}$×$\frac{1}{4}$=0.0125mol,通过导线的电量是0.0125mol×4×6.02×1023×1.60×10-19=0.482×10-4;n(HNO3)=0.05mol,则c(HNO3)=$\frac{0.05mol}{0.5L}$=0.1mol/L,pH=1,丙池某电极析出1.60g某金属,氧化性比氢离子强的金属离子均可能,则BD符合,
故答案为:1;0.482×10-4;BD.
点评 本题考查原电池和电解池,明确发生的电极反应、离子的放电顺序即可解答,注意电子守恒在计算中的应用,题目难度中等,注重了基础知识的考查.


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 可以用铝热反应制得单质镁 | |
| B. | 从海带中提取碘常用过氧化氢做还原剂 | |
| C. | 水华、赤潮等水体污染是由于含氮、磷的大量污水任意排放造成的 | |
| D. | 铝热剂就是指铝和氧化铁混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
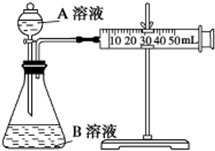 甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.
甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.| 序号 | A溶液 | B溶液 |
| ① | 2mL 0.1mol/L H2C2O4溶液 | 4mL 0.01mol/L KMnO4酸性溶液 |
| ② | 2mL 0.2mol/L H2C2O4溶液 | 4mL 0.01mol/L KMnO4酸性溶液 |
| ③ | 2mL 0.2mol/L H2C2O4溶液 | 4mL 0.01mol/L KMnO4酸性溶液和少量MnSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2 L CH3CH2OH中含有的分子数目为0.5NA | |
| B. | 14g分子式为CnH2n的链烃中含有的C-H键的数目为2NA | |
| C. | 室温时,1.0 L pH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA | |
| D. | Fe与水蒸气反应生成22.4L氢气,转移电子数为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com