
| 温度 | pH=7 | pH=6 | pH=5 | pH=3 |
| 20℃ | 300 | 240 | 160 | 58 |
| 30℃ | 160 | 108 | 40 | 20 |
| 50℃ | 80 | 50 | x | 8 |
| A. | x可能为42 | |
| B. | 其他条件不变,在30°、pH=4下的反应速度比40℃、pH=6时快 | |
| C. | 根据单一变量法,无法比较温度、pH均不同的两组实验的反应速率较慢 | |
| D. | 30℃,pH=3条件下,KI的反应速率为v(KI)=0.005mol•L-1•s-1 |
分析 影响在溶液里发生的化学反应的反应速率,外界因素主要的温度、浓度及溶液的pH,并且温度越高反应速率越高,浓度越大反应速率越快,在相同温度下,溶液的pH越小,反应速率越快,据此分析解答.
解答 解:A.在相同pH的条件下,温度越高,反应速率越快,所需要时间越短,则x应小于40,故A不选;
B.30°、pH=4和40℃、pH=6是两个不同的条件下进行的反应,结合温度越高反应速率越快,pH越小反应速率越快,因此无法比较,故B不选;
C.结合温度越高反应速率越快,pH越小反应速率越快,根据单一变量法,无法比较温度、pH均不同的两组实验的反应速率较慢,故C选;
D.30℃,pH=3条件下,只知道反应进行所需要的时间,不知道反应物或生成物的变化浓度,无法计算反应速率,故D不选;
故选:C.
点评 本题是探究影响在溶液里发生的化学反应的反应速率的因素,要在其它条件相同的情况下比较某一因素对反应的影响,基础性考查,难度不大,只要认真分析,挖掘信息,能快速解答.


 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:选择题
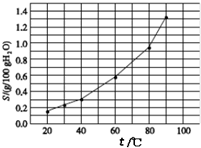
| A. | 温度升高不利于溴酸银的溶解 | |
| B. | 溴酸银的溶解是放热过程 | |
| C. | 若硝酸钾中含有少量溴酸银,可用重结晶方法提纯 | |
| D. | 60℃时,将0.04g溴酸银加入到10g水中,形成的分散系中存在沉淀溶解平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烷 | B. | 乙醇 | C. | 乙酸 | D. | 蔗糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
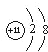 阴离子和Ba(NO3)2反应生成不溶于盐酸的白色沉淀.D的浓溶液与KMnO4混合,生成的气体能使石蕊溶液褪色,A的水溶液显酸性.用化学式表示A、B、C、D、E各是什么物质.写出有关化学方程式.
阴离子和Ba(NO3)2反应生成不溶于盐酸的白色沉淀.D的浓溶液与KMnO4混合,生成的气体能使石蕊溶液褪色,A的水溶液显酸性.用化学式表示A、B、C、D、E各是什么物质.写出有关化学方程式.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 其他步骤正确,滴定达到终点时,俯视读数,测得c(H+)偏大 | |
| B. | 实验测得25℃时,HgI2的Ksp=4×10-9 | |
| C. | 一定温度下,向HgI2饱和溶液中加入少量Hg(NO3)2溶液,HgI2的Ksp减小 | |
| D. | 温度不变,在t时,向HgI2饱和溶液中加入少量浓KI溶液,离子浓度变化如图所示 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
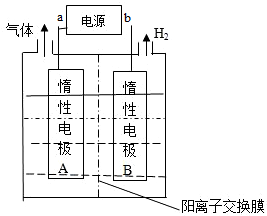
| A. | 外加电源的a极为正极 | |
| B. | 电解过程中,Li+向B极迁移 | |
| C. | 阳极反应式为:4OH--4e-═O2↑+H2O | |
| D. | 每生成1molLiOH,外电路转移1mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
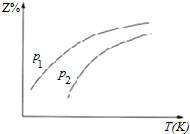
| A. | △H<0 | |
| B. | 若p1>p2,则Y一定呈气态 | |
| C. | 升高温度,该反应的化学平衡常数减小 | |
| D. | 反应处于平衡状态时,有c(X):c(2)=1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| CH4 (g) | H2O (g) | CO (g) | H2 (g) |
| 3.0mol•L-1 | 8.5mol•L-1 | 2.0mol•L-1 | 2.0mol•L-1 |
| 实验序号 | 温度/℃ | 压强/kPa | v(CH4)/mol•L-1•s-1 | v(H2O)/mol•L-1•s-1 |
| 1 | 360 | P1 | 0.100 | 0.100 |
| 2 | 480 | 101 | 0.120 | 0.120 |
| 3 | 360 | P2 | 0.080 | 0.080 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com