
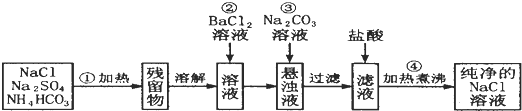
���� ���������ơ�̼����淋��Ȼ��ƹ��壬�����̿�֪�����з������������·ֽⷴӦ���ֽ��Ĺ�������ˮ�����Ȼ�����Ӧ��ȥ��������ӣ�������̼���Ƴ�ȥ�����ı����ӣ����˺���Һ�к�NaCl��̼���ƣ��������ȥ̼���ƺ�����ΪNaCl�������õ�������NaCl���Դ������
��� �⣺��1�����ȹ��壬Ӧ�������н��У��ʴ�Ϊ��������
��2������̼���ƣ������ڳ�ȥ������Ba2+����Ӧ�Ļ�ѧ����ʽΪNa2CO3+BaCl2=BaCO3��+2 NaCl�������������ᱵ�����������ʣ�
�ʴ�Ϊ����ȥ������Ba2+�� Na2CO3+BaCl2=BaCO3��+2 NaCl�������ԣ�����Ba��NO3��2��ʹ��Һ�������µ���������NO3-���Ժ����������ȥ��
��3������������ᣬ��Ӧ�����Һ�д��ڶ�����̼���Ȼ��⣬�ʴ�Ϊ����ȥ�ܽ�����Һ�е�CO2��HCl��
���� ���⿼����������ᴿʵ�鷽������ƣ�Ϊ��Ƶ���㣬���������еĻ�ѧ��Ӧ���������뷽��Ϊ���Ĺؼ������ط�����ʵ���������ƶ������Ŀ��飬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2NO2��g��?N2O4��g�� | B�� | 2HI��g��?H2��g��+I2��g�� | ||
| C�� | PCl5?PCl3��g��+Cl2��g�� | D�� | CaCO3��s��?CaO��g��+CO2 ��g�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��3 | B�� | 2��3 | C�� | 1��4 | D�� | 2��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �÷�Ӧ���û���Ӧ | B�� | �÷�Ӧ��FeCl3����ԭ�� | ||
| C�� | ��ԭ�ԣ�Fe��Cu | D�� | �����ԣ�CuCl2��FeCl3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na+ | B�� | Cu2+ | C�� | H+ | D�� | Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
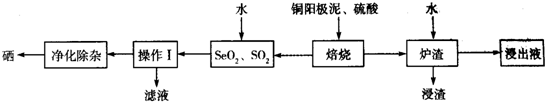

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
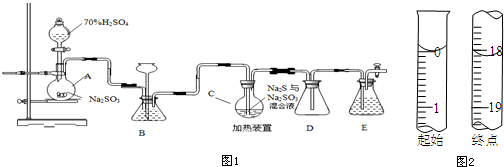
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ǻ벻�£�Ҫ��������˼� | B�� | ���������Ϊͭ | ||
| C�� | ���ϵ���˿����������ɻ���ʼ�� | D�� | ˮ��ʯ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com