
【题目】根据如图能量关系示意图,下列说法正确的是

A. 1 mol C(s)与1 mol O2(g)的能量之和为393.5 kJ
B. 反应2CO(g)+O2(g)= 2CO2(g)中,生成物的总能量大于反应物的总能量
C. 由C(s)→CO(g)的热化学方程式为:2C(s)+O2(g)= 2CO(g) ΔH=-221.2 kJ·mol-1
D. 热值指一定条件下单位质量的物质完全燃烧所放出热量,则CO热值ΔH=-10.1 kJ·mol-1
【答案】C
【解析】
由图可知,转化Ⅰ反应物总能量大于生成物总能量,为放热反应,热化学方程式为C(s)+O2(g)= CO2(g) ΔH=-393.5 kJ·mol-1,转化Ⅱ反应物总能量大于生成物总能量,为放热反应,热化学方程式为2CO(g)+O2(g)= 2CO2(g) ΔH=-282.9kJ·mol-1,转化Ⅰ—转化Ⅱ得C(s)→CO(g)的热化学方程式2C(s)+O2(g)= 2CO(g) ΔH=-221.2 kJ·mol-1。
A项、由图可知1 mol C(s)与1 mol O2(g)的能量比1 mol CO2(g)能量高393.5 kJ,故A错误;
B项、由图可知反应2CO(g)+O2(g)= 2CO2(g)为放热反应,生成物的总能量小于反应物的总能量,故B错误;
C项、由图可知1 mol C(s)与O2(g)生成1 mol CO(g)放出热量为393.5 kJ-282.9 kJ=110.6 kJ,则C(s)→CO(g)的热化学方程式为2C(s)+O2(g)= 2CO(g) ΔH=-221.2 kJ·mol-1,故C正确;
D项、热值指一定条件下单位质量的物质完全燃烧所放出热量,则CO的热值为282.9 kJ×![]() g≈10.1 kJ·g-1,故D错误;
g≈10.1 kJ·g-1,故D错误;
故选C。


科目:高中化学 来源: 题型:
【题目】有关晶体的结构如图所示,下列说法中不正确的是 ( )


A. 在NaCl晶体中,距Na+最近的Cl-形成正八面体
B. 在CaF2晶体中,每个晶胞平均占有4个Ca2+
C. 在金刚石晶体中,碳原子与碳碳键个数的比为1∶2
D. 该气态团簇分子的分子式为EF或FE
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)含有6.02×1023个H的H2O,其物质的量是________ mol;含有0.4 molAl3+的Al2(SO4)3溶液中所含SO42-的个数是________
(2)0.3 mol NH3分子中所含原子数与_______ molH2O分子中所含原子数相等。
(3)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为__________。
(4)某结晶水合物的化学式为A·nH2O,A的相对分子质量为M。如将a g该化合物加热至结晶水全部失去,剩余的残渣为b g,则n=________。
(5)在同温同压下,某气体X与H2气体的密度之比为14:1,则气体X的分子式可以是_______________(至少写出两种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】学习化学应该明白“从生活中来,到生活中去”道理,并加以实践。氯气是一种化学性质活泼的非金属单质,工业上可用氯气制取漂白粉、有机溶剂等。
(1)实验室中所用少量氯气常用下列方法制取:4HCl(浓)+MnO2![]() Cl2↑+MnCl2+2H2O。请将该反应改写成离子方程式:________________________________________。
Cl2↑+MnCl2+2H2O。请将该反应改写成离子方程式:________________________________________。
(2)甲同学设计如图所示装置研究氯气能否与水发生反应。气体X是含有少量空气和水蒸气的氯气。请回答下列问题:

①浓硫酸的作用是___________________________________________。
②证明氯气和水反应的实验现象为____________________________________________。
③此实验装置还不够完善,应该在D处添加的实验装置是_________________________,D处反应的化学方程式为__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取8.54 g含有Na2CO3、NaOH、Ba(NO3)2的固体混合物溶于足量水中,向反应后的试管中逐滴滴加1.00 mol·L-1的盐酸,加入盐酸的体积和沉淀质量的关系如图所示。

(1)混合物中Ba(NO3)2的物质的量至少为________mol。
(2)X的最大值为_________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气体的自动化检测中常应用根据原电池原理设计的传感器。下图为电池的工作示意图:气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号。下表列出了待测气体及敏感电极上部分反应产物。


则下列说法中正确的是
A. 上述气体检测时,敏感电极均作电池负极
B. 检测 Cl2 气体时,敏感电极的电极反应式为 Cl2+2e-=2Cl-
C. 检测 H2S 气体时,对电极充入空气,对电极上的电极反应式为 O2+2H2O+4e-=4OH-
D. 检测 Cl2 和 CO 体积分数相同的两份空气样本时,传感器上电流大小、方向相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员提出了由CO2 和 CH4 转化为高附加值产品CH3COOH 的催化反应历程如图所示:
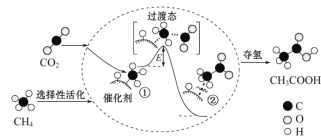
下列说法正确的是
A. 该反应证明任何非自发反应只要条件合适都能进行
B. 反应过程中,只有C—H 键发生断裂
C. 状态①、②之间的能量差即该反应的焓变
D. 合适的催化剂可有效降低活化能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:D为烃;E分子中碳元素与氢元素的质量之比6∶1,相对分子质量为44,其燃烧产物只有CO2和H2O。A的最简式与F相同,且能发生银镜反应,可由淀粉水解得到。

(1)A的结构简式为__________________。
(2)写出D→E的化学方程式:_______________________。
(3)下列说法正确的是____。
A.有机物F能使石蕊溶液变红
B.用新制的氢氧化铜无法区分有机物C、E、F的水溶液
C.等物质的量的C和D分别完全燃烧消耗氧气的量相等
D.可用饱和碳酸钠溶液除去有机物B中混有的少量C、F
E. B的同分异构体中能发生银镜反应的酯类共有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方程式书写正确的是
A.乙酸与乙醇的酯化反应:CH3COOH+C2H518OH![]() CH3COOC2H5+H218O
CH3COOC2H5+H218O
B.工业上冶炼铝:2AlCl3(熔融)![]() 2Al+3Cl2↑
2Al+3Cl2↑
C.甲烷与氯气产生一氯甲烷:CH4+Cl2![]() CH3Cl+HCl
CH3Cl+HCl
D.足量SO2通入澄清石灰水:SO2+Ca2++2OH-=CaSO3↓+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com